I løpet av de siste 10 – 15 årene har vår kunnskap om cytokrom P-450 (CYP)-systemet økt dramatisk. I dag er det kjent at variasjon i aktiviteten til legemiddelmetaboliserende enzymer i dette systemet kan forklare hvorfor noen har mangelfull effekt av legemidler, hvorfor noen får bivirkninger eller toksiske effekter av legemidler og hvorfor tilsynelatende ubeslektede legemidler interagerer med hverandre. Denne artikkelen presenterer bakgrunnen for hvorfor CYP-systemet er blitt karakterisert som den viktigste enkeltfaktoren som forklarer interindividuelle så vel som intraindividuelle variasjoner i legemiddeleffekt.
Cytokrom P-450 (CYP) er en fellesbetegnelse på en gruppe enzymer som kan bryte ned fettløselige stoffer til mer vannløselige aktive eller inaktive metabolitter som lettere skilles ut via nyrene (1). Enzymgruppens opprinnelige rolle er å uskadeliggjøre kroppsfremmede naturlig forekommende gifter, men også en rekke legemidler metaboliseres av CYP-systemet. CYP-enzymene er fremfor alt lokalisert i leveren, men finnes også i tarm, hjerte, hjerne og andre organer. Den første delen av navnet, cytokrom, skyldes enzymenes fargepigment som gir leveren dens karakteristiske brune farge. Den andre delen, P-450, kommer av at enzymene absorberer lys med en bølgelengde på rundt 450 nm. Hos mennesket finnes mer enn 50 ulike CYP-enzymer, men færre enn ti av disse har noen kjent betydning når det gjelder å bryte ned legemidler (1). De viktigste legemiddelmetaboliserende enzymene presenteres i tabell 1.
|
Tabell 1 De viktigste legemiddelmetaboliserende cytokrom P-450 (CYP)-enzymene med eksempler på legemidler som hovedsakelig metaboliseres av, eller hemmer eller induserer de ulike enzymene
|
|
Enzym
|
Genotyping tilgjengelig
|
Legemidler som metaboliseres
|
Legemidler som hemmer
|
Legemidler som induserer
|
|
CYP1A2
|
Nei
|
Klozapin, koffein, olanzapin, tamoksifen, teofyllin, trisykliske antidepressiver
|
Ciprofloksacin, fluvoksamin, verapamil
|
”Klassiske”¹
|
|
CYP2C9
|
Ja
|
Fenytoin, glibenklamid, glipizid, losartan, mikonazol, NSAID-preparater², warfarin
|
Amiodaron³, flukonazol
|
”Klassiske”¹
|
|
CYP2C19
|
Ja
|
Citalopram, diazepam, karisoprodol, moklobemid, omeprazol, proguanil⁴, propranolol, trisykliske antidepressiver
|
Fluvoksamin
|
”Klassiske”1,³
|
|
CYP2D6
|
Ja
|
Alprenolol, flekainid, fluoksetin, fluvoksamin, haloperidol, kodein⁴, metoprolol, meksiletin, mianserin, paroxetin, perfenazin, risperidon, tioridazin, trisykliske antidepressiver, timolol, tropisetron, venlafaxin, zuklopentixol
|
Bupropion, fluoxetin, paroxetin, visse antipsykotika
|
Ingen
|
|
CYP2E1
|
Nei
|
Enfluran, etanol, halotan, paracetamol
|
Etanol⁵
|
”Klassiske”1,³, etanol⁵
|
|
CYP3A4
|
Nei
|
Alprazolam, amlodipin, buspiron, cisaprid, doksorubicin, ciklosporin, diltiazem, erytromycin, etoposid, felodipin, ifosfamid, indinavir, isradipin, itrakonazol, ketokonazol, klaritromycin, lovastatin, midazolam, nefazodon, nelfinavir, nifedipin, nimodipin, p-piller (etinyløstradiol), ritonavir, saquinavir, sildenafil, simvastatin, takrolimus, tamoksifen, terfenadin, verapamil, vinblastin, zopiklon
|
Erytromycin, diltiazem, itrakonazol, ketokonazol, klaritromycin, mikonazol, nefazodon, ritonavir, verapamil
|
”Klassiske”¹
|
1 Barbiturater, fenytoin, johannesurt, karbamazepin, rifampicin 2 Ikke-steroide antiinflammatoriske midler 3 Relativt svak påvirkning 4 Substansen som sådan er inaktiv, men har en farmakologisk aktiv metabolitt. En hemning av legemidlets metabolisme vil dermed kunne gi en nedsatt klinisk effekt 5 Etanol kan både hemme og indusere avhengig av om det dreier seg om et akutt inntak (hemmer) eller et kronisk inntak (induserer) |
Den metabolske aktiviteten til enzymene varierer i betydelig grad fra person til person; det er ikke uvanlig med 10 – 20 gangers variasjon i enzymaktivitet mellom ulike individer. Dette betyr at for å oppnå samme legemiddelkonsentrasjon i plasma, må dosen hos dem som bryter ned et legemiddel med størst hastighet være 10 – 20 ganger høyere enn hos dem som bryter ned legemidlet langsomst. Gir man en vanlig, anbefalt gjennomsnittsdose til dem som bryter ned legemidlet langsomst, vil høye plasmakonsentrasjoner og risiko for bivirkninger og toksiske effekter bli resultatet. For å få optimal effekt må disse individene bruke langt lavere doser enn det som anbefales. Gir man en gjennomsnittsdose til dem som bryter ned legemidlet raskest, vil manglende klinisk effekt bli resultatet. Siden legemiddelkonsentrasjonen i plasma hos disse pasientene vil være lav, kan de uberettiget bli beskyldt for ikke å ta legemidlet som forskrevet.
Genetisk bestemt metabolisme
Den metabolske kapasiteten til tre av de viktigste enzymene, CYP2C9, CYP2C19 og CYP2D6, er genetisk bestemt (2, 3). Henholdsvis< 1 %, 3 – 4 % og 7 % i befolkningen, såkalte langsomme omsettere, har inaktiverende mutasjoner i begge genene som koder for det respektive enzym (fig 1). Ved å identifisere personer med inaktivt enzym og behandle disse med lave doser av de legemidlene som brytes ned av det aktuelle enzymet, vil man forebygge bivirkninger samtidig som den terapeutiske effekten opprettholdes. Et eksempel på dette er at genetisk testing for CYP2C9-aktivitet kan forhindre blødningskomplikasjoner hos pasienter som behandles med warfarin (4).
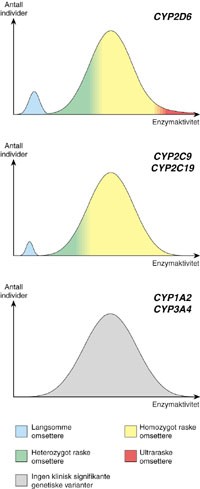
Figur 1 Frekvensfordeling av enzymaktivitet i befolkningen for cytokrom P-450-enzymene CYP2D6 (øverst), CYP2C9 og CYP2C19 (i midten), og CYP1A2 og CYP3A4 (nederst)
Personer som har ett mutert og ett normalt gen, såkalt heterozygot raske omsettere, vil bryte ned legemidler via det aktuelle enzymet med en hastighet som er innenfor normalvariasjonen, men som kan være noe langsommere enn gjennomsnittet (fig 1). Personer med to gener som koder for aktivt enzym, såkalt homozygot raske omsettere, vil bryte ned legemidler via det aktuelle enzymet med normal hastighet (fig 1).
For CYP2D6, men ikke for de andre enzymene, er det vist at noen få prosent i befolkningen har mer enn to normale genkopier. Disse individene, såkalte ultraraske omsettere, vil ha store mengder av dette enzymet og vil dermed bryte ned legemidler via CYP2D6 med svært høy hastighet (fig 1). For å få optimal effekt må disse individene bruke til dels langt høyere doser av de aktuelle legemidlene enn det som anbefales.
Den nevnte frekvensfordelingen av langsomme og ultraraske omsettere er basert på norsk og vesteuropeisk (kaukasisk) befolkning. Forekomsten varierer imidlertid betydelig mellom ulike etniske grupper. For eksempel er frekvensen av ultraraske omsettere for CYP2D6 ca. 20 % i befolkningsgrupper på den arabiske halvøy og i ØstAfrika (ca. 2 – 4% i Norge), mens forekomsten av langsomme omsettere for CYP2C19 er rundt 20 % i Øst-Asia og opptil 70 % på enkelte stillehavsøyer (3 – 4% i Norge).
Genetisk testing (genotyping) av CYP2C9, CYP2C19 og CYP2D6 utføres nå rutinemessig flere steder i landet. Til analysen trengs noen få milliliter fullblod.
Påvirkning av omgivelsesfaktorer
En genotyping gir svar på individets genetisk bestemte kapasitet til å bryte ned legemidler via det aktuelle enzymet. Enzymaktiviteten påvirkes imidlertid også av faktorer som for eksempel mat, drikke, infeksjoner og graviditet, samt av inntak av legemidler som hemmer eller øker enzymets kapasitet (1 – 3) (tab 1). Denne typen påvirkning kan ikke oppdages ved genotyping, men kan bedømmes ved å måle serumkonsentrasjonen av et av de legemidlene som brytes ned av det aktuelle enzymet.
For noen CYP-enzymer, som CYP1A2 og CYP3A4, er det ikke identifisert mutasjoner som har klinisk betydning. Likevel er det en betydelig variasjon i aktiviteten også av disse enzymene (fig 1). Tobakksrøyk inneholder stoffer som induserer aktiviteten til CYP1A2 (5). Røykere får dermed lavere konsentrasjoner av legemidler som brytes ned av CYP1A2 (tab 1) og behøver derfor høyere doser av disse legemidlene for å få samme kliniske effekt som ikke-røykere. Grapefruktjuice, men ikke andre typer juice, inneholder substanser som hemmer CYP3A4. Etter inntak av grapefruktjuice stiger konsentrasjonen av legemidler som brytes ned av CYP3A4, noe som kan medføre at det oppstår toksiske effekter som f.eks. nyreskade av ciklosporin ved samtidig ciklosporinbehandling (6).
Legemiddelinteraksjoner
Interaksjoner oppstår når et legemiddel som påvirker aktiviteten til et CYP-enzym kombineres med et annet legemiddel som metaboliseres av det samme enzymet. En rekke legemidler kan indusere eller hemme CYP-enzymenes aktivitet (tab 1) (3). Resultatet blir en lavere konsentrasjon med nedsatt terapeutisk effekt av det legemidlet som har fått sin metabolisme indusert, eller en økt konsentrasjon med risiko for bivirkninger og toksiske effekter av det legemidlet som har fått sin metabolisme hemmet. I enkelte tilfeller kan konsekvensene bli betydelige, som for eksempel alvorlige hjerterytmeforstyrrelser av terfenadin ved kombinasjonsbehandling med erytromycin (7), eller manglende graviditetsbeskyttelse av p-piller ved samtidig behandling med karbamazepin eller fenytoin (8).
Også naturmidler kan gi opphav til interaksjoner via påvirkning av CYP-aktiviteten. Et slikt eksempel er naturlegemidlet johannesurt, som er en kraftig induktor av blant annet CYP3A4 og CYP2C9 (9). Behandlingssvikt med til dels alvorlige konsekvenser er rapportert ved kombinasjonsbehandling med ciklosporin (rejeksjon etter organtransplantasjon), anti-HIV-midler (forverring av HIV-infeksjonen), eller warfarin (nedsatt antikoagulasjonseffekt).
Konklusjon
Kjennskap til CYP-systemet er viktig fordi man ut fra aktiviteten til de ulike CYP-enzymene kan skreddersy legemiddeldosen til hvert enkelt individ. Den enorme variabiliteten i nedbrytningshastighet forklarer også hvorfor noen pasienter må ha langt under anbefalt dose for å unngå bivirkninger, mens andre må ha langt over anbefalt dose for i det hele tatt å få noen klinisk effekt.
Spalten er redigert av Olav Spigset i samarbeid med Avdeling for legemidler ved Regionsykehuset i Trondheim og de øvrige klinisk farmakologiske miljøene i Norge
Se også kunnskapsprøve på www.tidsskriftet.no/quiz