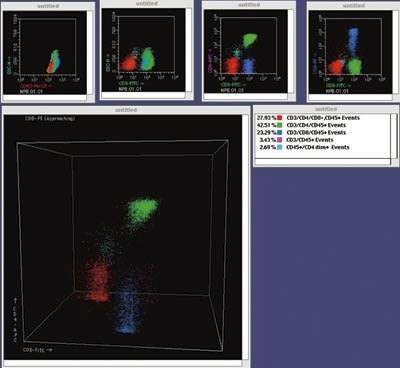
Immunfenotypisk påvisning av tre subpopulasjoner av T-lymfocytter i væskestrømscytometri. Hver akse representerer uttrykk av et antigen. Med tredimensjonalt plott (det store bildet) kan hver populasjon undersøkes for tre antigener samtidig. Foto Husebekk og medarbeidere
Spesialiteten Immunhematologi og medisinsk immunologi ble unnfanget for 30 år siden ved fusjon mellom to laboratoriefag. Senere har den skiftet navn til Immunologi og transfusjonsmedisin som uttrykk for økende integrasjon og kontakt med klinisk virksomhet.
Utviklingen etter 1980
Transfusjonsmedisinen har fokusert på å dekke behovet for trygge blodprodukter og utføre sikre immunhematologiske undersøkelser. Oppdeling av giverblodet i komponenter ble fra slutten av 1970-årene drevet frem av behovet for faktor VIII-holdig kryopresipitat til behandling av hemofili A-pasienter. Nasjonal selvforsyning gjorde at norske blødere slapp forholdsvis lett unna HIV/AIDS-epidemien. Arbeidet med å sikre alle blodprodukter mot virusoverføring førte til nasjonal samhandling om retningslinjer for transfusjonstjenesten, kvalitetssikring, infeksjonstesting og plasmafraksjonering. Komponentproduksjonen ble oppgradert til farmasøytisk nivå, og fra 1997 ble alle celleholdige blodkomponenter leukocyttfiltrert.
Norge fikk med dette en av verdens sikreste transfusjonstjenester. Det har imidlertid vært lite diskusjon omkring kliniske indikasjoner for transfusjon, og den kliniske betydningen av forandringene som inntrer i celleholdige blodprodukter ved lagring, er ikke blitt tilfredsstillende klarlagt.
Immunologi. Her har forskning ført til store gjennombrudd og åpnet for sofistikerte metoder for diagnostikk, behandling og oppfølging av pasienter. Undersøkelser for autoimmunitet er blitt tiltakende spesifikke og klinisk nyttige. Etterspørselen etter allergidiagnostikk øker stadig. Væskestrømscytometri fikk plass i spesialiteten tidlig i 1980-årene, og immunfenotyping ved leukemier og lymfomer er nå etablert ved alle universitetsavdelinger.
Forskningen har også ført til identifikasjon av HLA-komplekset. God HLA-forlikelighet mellom giver og mottaker ved allogene organ- og stamcelletransplantasjoner sikrer godt resultat. Det er også vist at noen HLA-molekyler disponerer sterkt for utvikling av autoimmune sykdommer. Dette brukes diagnostisk, og er også blitt et meget aktivt forskningsfelt i Norge.
Autolog stamcelletransplantasjon utføres ved de fleste universitetssykehusene som del av avansert kreftbehandling, og spesialister i Immunologi og transfusjonsmedisin har fått en sentral, pasientnær rolle i denne virksomheten. I 1970-årene var det forventninger til at immunapparatet skulle kunne stimuleres til effektivt å drepe cancerceller, men et generelt gjennombrudd her har latt vente på seg.
Forventninger til de neste 25 årene
Transfusjon av erytrocytter og trombocytter vil forbli en viktig del av behandlingen av kritisk syke pasienter, men indikasjonene vil bli satt ut fra mer kunnskapsbaserte kriterier enn i dag. Man kan neppe vente at alternativer til erytrocytter (hemoglobinløsninger, kunstige oksygenbærere) vil få annet enn nisjeanvendelser, og det er ingen utsikter til gode alternativer til trombocytt-transfusjon. Blodproduktene vil inneholde celler med bedre funksjonelle egenskaper enn i dag, og patogener vil kunne inaktiveres i enkeltblodposer.
Flere plasmaprodukter vil bli erstattet av molekylærbiologisk fremstilte produkter, og hemostaseregulerende preparater vil ha en mer etablert plass i traumatologien. Det ser ikke ut til at immunglobulin kan fremstilles godt nok molekylærbiologisk, og man kan derfor neppe vente gode alternativer til plasmaderiverte gammaglobulinpreparater.
Blodbankene vil bestå, men tapping og komponentfremstilling vil skje mer automatisert. Gen- og proteinbaserte microarrays vil gjøre blodtyping mer nøyaktig. Databasert identitetssikring av givere og mottakere vil minimalisere feiltransfusjoner. For gravide vil det i tillegg til Rh-diagnostikk og profylakse være etablert overvåking og behandling for neonatal alloimmun trombocytopeni.
Immunologi. Immunfenotyping av leukemi- og lymfomceller vil være ytterligere utviklet og bidra til sikrere terapivalg, prognosevurdering og oppfølging av pasientene. Teknikker for påvisning av minimal restsykdom ved cancer vil være vel etablert. Det vil være utviklet flere monoklonale antistoffer mot overflatemarkører på cancerceller, og immunterapi vil være etablert som et supplement til mer konvensjonell behandling av cancer. Kreftvaksiner vil være tilgjengelige for definerte tilstander og kreve individualisert cellemanipulering ex vivo. Avanserte genteknologiske typemetoder, også for påvisning av andre relevante molekyler enn HLA, vil være tatt i bruk i transplantasjonsimmunologiske utredninger.
Til diagnostikk og oppfølging av pasienter med autoimmune sykdommer vil flere klinisk relevante tester være utviklet. Luminex-teknologi, hvor mange undersøkelser kan utføres samtidig i samme prøve, er på vei inn som alternativ til etablert ELISA-metodikk. Det vil sannsynligvis være utviklet metoder til å forhindre at individer med høy risiko for å utvikle autoimmune sykdommer får sykdom («predict and prevent»). Også genterapi kan være etablert og integrert i fagets pasientnære virksomhet
Større avdelinger vil utføre celleterapi med stamceller av ulike typer (bruskceller, mesenkymale celler etc.).
Sluttbemerkninger
Videre utvikling av laboratoriemedisinen er en viktig forutsetning for utvikling av klinisk medisin. Fagfeltet Immunologi og transfusjonsmedisin har i så måte et stort potensial. Norge har sterke forskningsmiljøer som vil kunne gi viktige bidrag til utviklingen. Om 25 år tror vi at faget vil være mer integrert i den daglige kliniske virksomheten og utgjøre en grunnleggende forutsetning for avansert diagnostikk og behandling. Faget vil oppleves som et naturlig hele der spesialistene undersøker og manipulerer celler og cellegenererte produkter til klinisk anvendelse og til dels deltar direkte i pasientbehandlingen. Vi tror at spesialiteten vil hete «Immunologi og celleterapi».