Vi var flere som på medisinstudiet fikk en aha-opplevelse da vi endelig kom til 9. termin og patologien. I «lille» Robbins Basic pathology (1) kunne vi se hvordan betennelsescellene gikk til angrep på myokardfibrene ved et hjerteinfarkt eller steatosen som bredte seg i leveren etter for stort alkoholinntak. Enkelte av oss forble i faget.
Patologi er læren om sykdommer og sykdomsprosesser, studert i celler og vev. Faget har utviklet seg gjennom mer enn tusen år. År 980 obduserte Avicenna krigsmenn i Iran, resultatene ble nedskrevet på arabisk i et medisinsk leksikon. I 1543 ble obduksjonsfunn systematisert av Andreas Vesalius, belgisk anatom og lege, i De humani corporis fabrica. Giovanni Batista Morgagni (1682 – 1771), professor i anatomi i Padua, beskrev i De sedibus causis morborum patologisk-anatomiske funn ved obduksjoner av mer enn 700 avdøde. Lysmikroskopet ble utviklet tidlig på 1600-tallet. Engelskmannen Robert Hooke (1635 – 1703) la en korkbit under mikroskopet og så små, boksliknende strukturer som minnet om cellene i et kloster – derav navnet. 200 år senere slo den tyske legen, patologen, biologen, historikeren og politikeren Rudolf Virchow (1821 – 1902) fast at alle celler kommer fra preeksisterende celler («omnis cellula e cellula») og at sykdom var forårsaket av endringer på cellenivå. Dermed grunnla han cellulærpatologien. Faget patologi gjorde et byks inn i den moderne medisin.
De første obduksjoner i Norge ble foretatt på 1700-tallet. Systematisk obduksjonsvirksomhet kom først i stand da Det Kgl. Frederiks Universitet i Christiania ble opprettet i 1811. Emmanuel Winge (1827 – 94) fikk det første professoratet i patologi i 1866. Han ble etterfulgt av Hjalmar Heiberg (1837 – 97). Under dennes ledelse ble det første patologibygget i Norge oppført i 1879 ved Rikshospitalet. I dag har Norge 16 patologilaboratorier tilknyttet sykehus og fire private. I 2003 ble 301 686 biopsier og 575 252 cytologiske prøver undersøkt.
Faget patologi har endret seg betydelig de siste 100 år, men lysmikroskopisk vurdering av morfologisk tilstand har vært og er helt sentralt. Standardmetoden er fortsatt hematoksylin-eosin-farging av snitt fra parafininnstøpt materiale. Mengden vev diagnosene stilles på har derimot hatt en utvikling mot det minimalistiske – fra operasjonspreparater og kirurgiske biopsier til preoperativ diagnostikk med grovnålsbiopsier med 1 x 1 x 5 – 10 mm store vevssylindre eller eksfoliativ cytologi/finnålspunksjoner, hvor enkeltceller blir undersøkt.
Av stor betydning er den dramatiske utviklingen innen supplerende undersøkelser. Det første elektronmikroskopet ble bygd i 1931. Dette muliggjorde den ultrastrukturelle patologi, som fortsatt er til stor nytte, f.eks. innen nyresykdommer. De siste 20 år er patologifaget i stor grad blitt preget av fremskritt innen immunologi, kjemi og molekylærbiologi (2, 3). Immunhistokjemi med visualisering av antigen-antistoff-reaksjoner muliggjør påvisning av spesifikke celleprodukter. Metoden er i bruk ved alle patologilaboratorier og er uunnværlig innen bl.a. tumordiagnostikk og virusdiagnostikk. Ved hjelp av polymerasekjedereaksjon (PCR) kan RNA og DNA oppformeres ved hjelp av spesifikke prober direkte på vevssnitt. På denne måten kan genforandringer som karakteriserer forskjellige tumortyper avdekkes. Cytogenetisk undersøkelse av ferskt vev identifiserer karakteristiske kromosomforandringer. Kombinasjonen av immunhistokjemi og væskestrømscytometriske metoder kan karakterisere og sortere celler i løpet av sekunder.
I dag er kravene til diagnostikk helt andre enn for bare ti år siden. Patologens oppgave er ut fra mottatt vev å subklassifisere sykdommen, uttale seg om prognose, gi prediktiv informasjon med henblikk på videre behandling og eventuelt klassifisere behandlingsrespons. Dette krever utstrakt bruk av integrert diagnostikk, hvor morfologiske forhold sammenholdes med nødvendige supplerende undersøkelser. Et godt eksempel er hematopatologi (4). Subklassifisering av leukemi og lymfom baseres på morfologiske forhold, detaljert immunfenotyping og cytogenetiske analyser, i tillegg til spredningsmønster og kliniske funn. Dette danner basis for pasientbehandlingen. I dette arbeidet er patologen helt sentral. Et annet eksempel er brystkreft. Tumor klassifiseres morfologisk, og det gis en prognostisk gradering av tumors aggressivitet lysmikroskopisk på snitt. Deretter undersøkes tumor immunhistokjemisk for tilstedeværelse av hormonreseptorer, med tanke på sannsynlig nytte av hormonbehandling. Enkelte tumorer har amplifisert et onkogen kalt Her2, og selve proteinproduktet påvises immunhistokjemisk (fig 1). Ved tilstedeværerelse av Her2-produktet i cellemembranen får pasienten tilbud om behandling med herceptin, et monoklonalt antistoff rettet mot Her2-proteinet. Etter en samlet vurdering blir pasienten innlemmet i forskjellige behandlingsprotokoller. Det sier seg selv at ikke alle patologer kan beherske alle aspekter ved faget patologi like godt. Dette har fremtvunget en viss grad av ikke-formalisert subspesialisering, særlig innen tumordiagnostikk.
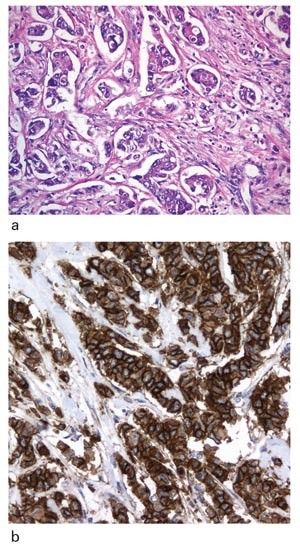
Figur 1 a) Hematoksylin-eosin-farget snitt av et infiltrerende duktalt mammakarsinom, histologisk grad 3, med b) immunhistokjemisk positivitet for Her2
Dagens forskning kan bli morgendagens rutineundersøkelser. De patologiske laboratoriene er rene gullgruver for fremtidige forskningsprosjekter. Her oppbevares rundt 40 millioner parafininnstøpte vevsprøver og cytologiske prøver. Dette utgjør prøver fra ti millioner pasienter og fem generasjoner nordmenn. Takket være nye metoder innenfor immunologi og molekylærbiologi kan dette arkivmaterialet nå undersøkes genetisk. Ny kunnskap og videre utvikling av dagens metodikk, som automatiserte mikroanalyser (mikrochips-, mikroarrayanalyser) og bioinformatikk, vil kunne føre til at behandlingen i større og større grad skreddersys for den enkelte pasient. Det vil kreve en redefinering av kravene til utdanning av patologer, som, i tillegg til morfologi, må kunne beherske fremtidens diagnostiske hjelpemidler.