Likvoré er en alvorlig tilstand fordi den innebærer risiko for bakteriell meningitt gjennom retrograd smitte fra nese, bihuler og øre. Likvoré viser seg vanligvis som rhinoré, men av og til også som otoré. Det er beskrevet okkulte fistler med lekkasje av cerebrospinalvæske som ikke behøver å gi symptomer på flere tiår. I noen tilfeller er en livstruende meningitt første indikasjon på at man må se etter en lekkasje av cerebrospinalvæske (1). Ikke påviste fistler kan dannes etter endoskopisk bihulekirurgi (2). Vi gir en oversikt over diagnostikk og behandling av likvoré basert på egen erfaring og en gjennomgang av utvalgt litteratur. Bruken av betasporprotein (beta-trace protein) som markør har modernisert diagnostikken.
Pasient 1. En 61 år gammel kvinne ble operert på grunn av kronisk sinusitt. Etter operasjonen rant det klar væske fra nesen og lekkasjen økte når hun bøyde seg fremover. Væsken inneholdt 42 mg/l betasporprotein, en verdi som er forenlig med likvoré. CT-undersøkelsen viste en beindefekt i sentrale lamina cribrosa. Det kunne ikke avgjøres om det forelå en ensidig eller en bilateral lekkasje. Hun ble operert endoskopisk med natriumfluoresceinfargeteknikk. Under operasjonen fant man lekkasje på begge sider av lamina cribrosa, og defektene ble dekket med frie transplantater av fascia lata (fig 1).
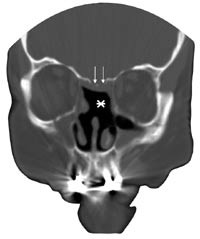
Figur 1 CT bihuler fire månder etter endonasal lukking av cerebrospinalvæskelekkasje (pasient 1). Øvre neseseptum er fjernet (asterisk). Beindefekter finnes på begge sider av lamina cribrosa (pilhoder)
Pasient 2. En 58 år gammel kvinne ble operert for tredje gang med transseptal, transsfenoidal tilgang for residiv av kromofobt hypofyseadenom. Pasienten hadde økende synsfeltsutfall, og adenomet vokste infiltrerende i skallebasis med gjennomvekst til sinus sphenoidalis. Etter inngrepet oppstod rhinoré, og CT caput viste pneumatocephalus. To endoskopiske operasjoner med transnasal tilgang ble gjennomført for å lukke lekkasjen, men begge var mislykte. CT-bilde viste en stor beindefekt i den fremre veggen og i gulvet av sella turcica (fig 2). Nesesekretet inneholdt 8,2 mg/l betasporprotein. Tredje forsøk på å lukke lekkasjen ble gjennomført med natriumfluoresceinfarging (fig 3). Defektene ble dekket med autolog fascia lata. På grunn av hydrocephalus ble det lagt en ventrikuloperitoneal shunt. Den postoperative CT-undersøkelsen viste ikke intrakranial luft, og ved kontroll etter fem måneder hadde hun ikke tegn til likvoré.
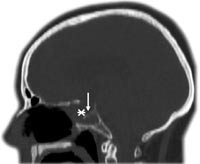
Figur 2 CT caput rekonstruert i parasagittalplan (pasient 2). Beindefekter finnes i fremre veggen (asterisk) og i gulvet av sella turcica (pilhode)
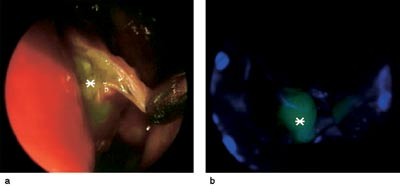
Figur 3 Intraoperativt endoskopisk bilde med fluorescerende cerebrospinalvæske (asterisk) i sinus sphenoidalis a) uten og b) med bruk av blåfilter og gulokular
Cerebrospinalvæskelekkasje kan være vanskelig å diagnostisere og behandle. Det finnes invasive og ikke-invasive diagnostiske metoder (3). Til de invasive hører CT-cisternografi, MR med intratekal gadolinium, farging med natriumfluorescein, liquorscintigrafi og digital subtraksjonscisternografi. De ikke-invasive metodene omfatter undersøkelse av væskeprøver for påvisning av liquormarkører, strømningssensitiv MR og kliniske undersøkelser. Undersøkelse av glukose i sekret er ikke lenger anbefalt (4). Dessverre finnes det ikke prospektive studier som viser prediksjonsverdiene av ulike undersøkelser for påvisning av likvoré, men beta ₂-transferrin ser ut til å være en pålitelig liquormarkør (5).
Betasporprotein
Siden 1960-årene har betasporproteinet vært kjent som et protein som er spesifikt for spinalvæsken (6). Senere fant man at betasporprotein og prostaglandin D-syntase er det samme proteinet (7). Det antas at betasporprotein spiller en sentral rolle i biokjemisk styring av søvn og våkenhet i den sentrale smertesansen (8, 9). Serum inneholder 0,3 mg/l betasporprotein, mens verdiene i cerebrospinalvæske angis til mellom 10 – 33 mg/l (tab 1) (10 – 16). Betasporprotein kan brukes i diagnostikk av likvoré. Forekomsten av betasporprotein måles i sekret fra nese eller øre kvantitativt ved hjelp av immunologisk lasernefelometri. Nødvendig prøvevolum er 5 µl. Analysetiden er ca. 20 minutter. En verdi på mer enn 6 mg/l er definert som forenlig med lekkasje av cerebrospinalvæske (15). I et materiale på 84 pasienter fant man at positiv prediktiv verdi av påvist betasporprotein i nese- eller øresekret var 1,0, mens negativ prediktiv verdi var 0,97 (17). Variasjonskoeffisient er mindre enn 4 % (16). Betasporprotein egner seg bedre enn beta₂-transferrin som markør i diagnostikken av likvoré.
|
Tabell 1 Kvantitative verdier av betasporprotein
|
|
Forfatter
|
Betasporprotein i serum (mg/l)
|
Betasporprotein i CSF (mg/l)
|
n
|
|
Link og Olsson 1972 (10)
|
ikke angitt
|
26 ± 6
|
59
|
|
Felgenhauer et al. 1987 (11)
|
ikke angitt
|
33 ± 11
|
192
|
|
Melegos et al. 1996 (12)
|
0,2 ± 0,07 (n = 33)
|
14,8 ± 6,9
|
12
|
|
Huber 2000 (13)
|
0,3
|
10
|
ikke angitt
|
|
Kleine et al. 2000 (14)
|
0,26
|
14,68
|
blandet
|
|
Petereit et al. 2001 (15)
|
0,5 (n = 34)
|
11 ± 2
|
20
|
|
Arrer et al. 2002 (16)
|
0,59 ± 0,2 (n =116)
|
19,6 ±5,8
|
19
|
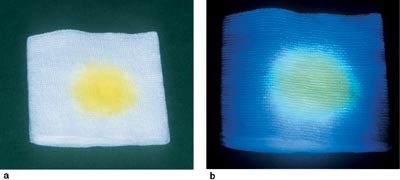
Figur 4 Fortynnet natriumfluorescein i a) daglys og b) under blålys
Natriumfluorescein
Fargeteknikken med bruk av natriumfluorescein ble først beskrevet i 1960 og senere utviklet videre (18, 19). Natriumfluorescein er et fargestoff som er tillatt til intravenøs eller oral bruk, men det er ikke beregnet som diagnostisk hjelpemiddel for intratekal injeksjon. Fargestoffet fordeler seg i intraduralrommet i løpet av noen timer etter lumbal injeksjon og blir utskilt renalt i løpet av tre dager. En fordel med natriumfluorescein er at det både kan brukes til å påvise om det foreligger en cerebrospinalvæskelekkasje og til å finne lekkasjestedet ved endoskopisk eller mikrokirurgisk kirurgi. Som bivirkninger ses forbigående svakhet i underekstremitetene, nummenhet, grand mal-anfall, opistotonus og hjernenervepareser (20). I et materiale på 925 pasienter fant man grand mal-anfall hos tre pasienter. Alle tre fikk natriumfluorescein injisert suboksipitalt (21). Alvorlige og varige bivirkninger er ikke beskrevet i litteraturen ved lumbal injeksjon og riktig dosering. Pasientene bør informeres om kjente bivirkninger og om mulige behandlingsalternativer. Ved bruk av natriumfluorescein legges en lumbaldrenasje dagen før inngrepet. 0,5 ml av en 10 % steril natriumfluoresceinløsning fortynnet med 10 ml autolog cerebrospinalvæske injiseres langsomt i spinalkanalen. Endoskopisk sporing av natriumfluorescein skjer ved hjelp av et blåfilter på lyskilden og et gulokular på endoskopet. Begge forsterker synligheten av fluorescensen (fig 4). Lumbaldrenet blir liggende i tre dager for å redusere det intrakraniale trykket den første tiden etter lukkingen av lekkasjen og dermed redusere faren for ny lekkasje.
Konklusjon
Diagnostikken av likvoré har to hovedaspekter: påvisning av cerebrospinalvæske og nøyaktig lokalisering av lekkasjestedet. Måling av betasporprotein anbefales for påvisning av cerebrospinalvæske. Lekkasjestedet lokaliseres best ved hjelp av bildediagnostikk. Når lekkasjestedet ikke kan lokaliseres nøyaktig, vil natriumfluoresceinfargeteknikk være til hjelp peroperativt. Kvantitativ måling av betasporprotein i ekstradurale væsker er en rask, presis, følsom og rimelig analytisk tilnærming til diagnostikk av likvoré. Kirurgisk lukning av cerebrospinalvæskelekkasje kan i de fleste tilfeller skje ved hjelp av endoskopisk nesekirurgi eller med ørekirurgisk teknikk. Figur 5 viser et flytdiagram for utredning av likvoré eller meningitt med mistanke om lekkasje av cerebrospinalvæske.
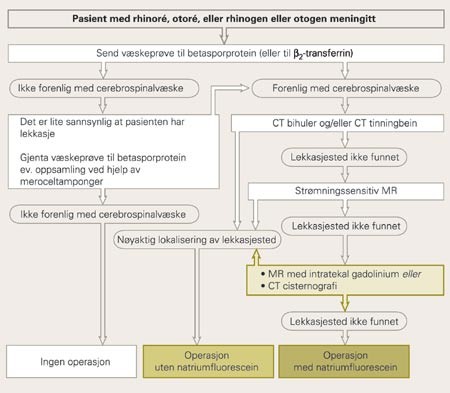
Flytdiagram som viser diagnostiske og terapeutiske prosedyrer. Grønn betyr invasiv diagnostikk eller terapi