Humant parvovirus B19-infeksjon opptrer i epidemier hvert tredje til sjette år. Viruset forårsaker erythema infectiosum eller den femte barnesykdommen. Hos barn gir infeksjonen oftest bare milde symptomer og utslett (1), mens voksne oftere får allmennsymptomer. Infeksjon i svangerskapet kan gi transplacentær smitte med alvorlig fostersykdom og -død som følge (1). En opphopning av tilfeller med alvorlig parvovirus B19-infeksjon i svangerskapet ved Kvinneklinikken, Haukeland Universitetssykehus, i løpet av en toårsperiode førte til en nærmere gjennomgang for å bedre rutinene. Vårt mål med denne artikkelen er å høyne bevisstheten om infeksjonen og de følger den kan gi i svangerskapet ved å beskrive kasuistikker og undersøke hvor stor mottakeligheten for infeksjon er blant gravide.
Materiale og metode
Parvovirus B19-infeksjon i svangerskapet belyses ved hjelp av fem tilfeller av alvorlig føtal infeksjon i løpet av 2001 – 02.
Vi brukte månedsmeldinger for laboratoriediagnoser (Nasjonalt folkehelseinstitutt) og registreringer ved Avdeling for mikrobiologi og immunologi, Haukeland Universitetssykehus, for å kartlegge antall pasienter med påvist IgM-antistoff mot parvovirus B19 som uttrykk for infeksjonshyppigheten i befolkningen gjennom året.
For å få vite hvor stor del av den gravide populasjonen som er mottakelig for infeksjonen, ble 206 serumprøver fra like mange kvinner våren 2003 undersøkt for IgG-antistoff mot parvovirus B19 med en enzymimmunologisk metode (Biotrin Parvovirus B19 IgG Enzyme Immunoassay, Biotrin International Ltd., Dublin, Irland). For å påvise parvovirus B19-DNA ble polymerasekjedereaksjon benyttet. Noen av disse undersøkelsene ble utført ved Nasjonalt folkehelseinstitutt (Helvi Holm Samdal, personlig meddelelse).
Pasient 1. I 18. svangerskapsuke ble perikardvæske hos fosteret påvist i forbindelse med rutineundersøkelse. Det forelå en ekkogen 8 mm stor tumor i høyre forkammer, leverforstørrelse og polyhydramnion, men ingen ekkokardiografiske tegn på hjertesvikt eller anemi. I 26. svangerskapsuke var alle forandringer gått tilbake, og ved kardiologisk undersøkelse av barnet etter fødselen var det ingen patologiske funn. I serum fra mor ble det påvist IgG-og IgM-antistoff – forenlig med aktuell infeksjon.
Pasient 2. Det ble i svangerskapsuke 26 påvist ascites hos fosteret. Videre utredning avdekket kardiomegali og nedsatt kontraktilitet, perikard- og pleuravæske, forstørret lever og placentaødem. Blodstrømsmålinger i a. cerebri media tydet på anemi, og kordocentese bekreftet dette (Hb 7,2 g/100 ml). Blodstrømsmåling i ductus venosus viste forhøyede hastigheter, forenlig med portahypertensjon. Etter to intrauterine transfusjoner gikk forandringene tilbake. Ved utskrivning fra barneavdelingen var barnet friskt, og det var ingen tegn på kardiale eller nevrologiske sekveler. Diagnosen ble bekreftet med serologiske undersøkelser og påvisning av parvovirus B19-DNA i mors serum ved polymerasekjedereaksjon.
Pasient 3. En gravid kvinne ble syk i 12. svangerskapsuke med feber, utslett og senere leddsmerter. I serum fra mor ble det etter hvert påvist IgG- og IgM-antistoff mot parvovirus B19, forenlig med aktuell infeksjon. Da hun i 25. svangerskapsuke kjente mindre liv, ble hun utredet nærmere og fikk påvist føtal ascites (fig 1), subkutant ødem, placentaødem, leverforstørrelse, intrakraniale forandringer forenlig med hjerneødem, ekkogene nyrer og tom urinblære. Kardiomegali, perikardeffusjon, lekkasje gjennom mitral- og trikuspidalklaffen og økt pulsatilitet i prekordiale vener tydet på hjertesvikt (fig 2). Forhøyede blodstrømshastigheter i a. cerebri media tydet på anemi. Blodprøve fra navlesnoren bekreftet anemi (Hb 1,9 g/100 ml) og trombocytopeni (Trc 17 · 10⁹/l). Fosteret fikk transfusjoner, men døde. Underveis hadde det utviklet seg ventrikkelseptumdefekt (fig 1). Parvovirus B19-DNA ble påvist ved polymerasekjedereaksjon i fosterblod, fostervann og placenta samt i mors serum.
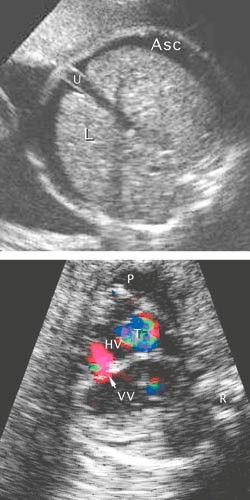
Figur 1 Øverst: Tverrsnitt av fosterbuken fremstilt med ultralyd i 25. svangerskapsuke viser ascites (Asc) som et av tegnene ved hydrops foetalis. Nederst: Fargedoppler av fosterhjertet viser en nylig oppstått ventrikkelseptumdefekt (pil) i forbindelse med parvovirus B19-infeksjon. Blod shuntes (rødt) fra venstre ventrikkel (VV) til høyre (HV). Det er kardiomegali og perikardeffusjon (P). Det ses også lekkasje i trikuspidalklaffen (T). L = lever, R = ryggsøyle, U = intraabdominal umbilikalvene
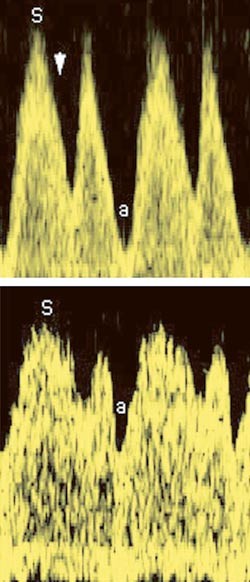
Figur 2 Øverst: Dopplermåling i ductus venosus ved parvovirus B19-infeksjon i 25. svangerskapsuke viser to tegn på føtal hjertesvikt: en aksentuert atriekontraksjonsbølge (a) og en bratt hastighetsreduksjon (pil) i siste delen av ventrikkelsystolen (S), noe som tilskrives redusert tøybarhet i myokard. Nederst: normal registrering til sammenlikning
Pasient 4. I 24. svangerskapsuke ble det med ultralydundersøkelse påvist subkutant ødem hos fosteret, ascites, perikardvæske, trikuspidal-lekkasje, fortykket vegg i ventrikkel og atrie, samt økt ekkogenitet i myokard. Måling av blodstrøm i a. cerebri media og ductus venosus tydet på henholdsvis anemi og hjertesvikt. Kordocentese bekreftet alvorlig anemi (Hb 2,2 g/100 ml) og trombocytopeni (Trc 29 · 10⁹/l). Etter fem intrauterine transfusjoner gikk hydrops tilbake, og hjertefunksjonen ble normalisert. I 28. svangerskapsuke ble mor forløst med keisersnitt pga mistanke om morkakeløsning. Barnet hadde Hb 12,3 g/100 ml og Trc 45 · 10⁹/l og fikk flere transfusjoner postnatalt. Ved utskrivning 11 uker senere var det fortsatt antatt aktiv parvovirus B19-infeksjon med fallende hemoglobinverdier. Barnet fikk påvist nedsatt hørsel på høyre øre, retinopati og dobbeltsidig lyskebrokk. Diagnosen ble bekreftet ved serologiske undersøkelser av mor og påvisning av virus-DNA i fosterblod.
Pasient 5. I forbindelse med ultralydundersøkelse i 18. svangerskapsuke ble det hos fosteret påvist hydrops og reduserte fosterbevegelser. Dopplermålinger av blodstrøm i a. cerebri media tydet på anemi, og kordocentese viste Hb 8,3 g/100 ml. Blodtrømsmålinger i ductus venosus og a. hepatica tydet på leveraffeksjon. Ved kontroll en uke senere var fosteret dødt. Resultatet av serologiske prøver fra mor var forenlig med aktuell infeksjon, men parvovirus B19-DNA ble ikke påvist i thoraxvæske.
Tre av kvinnene hadde hatt symptomer på virusinfeksjon tidlig i svangerskapet, og to av disse hadde vært utsatt for smitte og mistenkte selv parvovirus B19-infeksjon. Det gikk likevel henholdsvis seks, åtte og 13 uker før disse kom til ultralydundersøkelse. To av mødrene arbeidet med barn, to hadde barn i skolealder.
Laboratorieresultater
I 2001 ble det i 51 av 710 rekvirerte serumprøver påvist IgM-antistoff mot parvovirus B19 ved Avdeling for mikrobiologi og immunologi, Haukeland Universitetssykehus. For 2002 var de tilsvarende tallene 41 av 764 prøver. I hele landet ble det i 2001 og 2002 funnet henholdsvis 390 og 202 pasientprøver med påvist IgM-antistoff (fig 3).
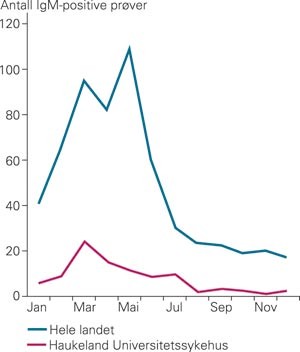
Årstidsvariasjonen for påvisning av IgM-antistoff mot parvovirus B19 ved Haukeland Universitetssykehus og for hele landet i 2001 – 02 (statistikk tatt fra månedsmeldinger for laboratoriediagnoser i Norge og avdelingens egne registreringer)
Ved serologisk undersøkelse av 206 gravide kvinner hadde 74 (35,9 %) ikke IgG-antistoff mot parvovirus B19 og var følgelig mottakelige for smitte.
Diskusjon
Humant parvovirus B19 er alminnelig utbredt globalt. Infeksjon opptrer i epidemier, med oppsving på ettervinteren (fig 3). Gjennomgått infeksjon gir livslang immunitet. Prevalensen av IgG-antistoff er rapportert å være 30 – 60 % hos voksne (2), noe som samsvarer med våre tall.
Serokonversjonsraten for kvinner i fertil alder i endemiske perioder er 1,5 % per år, men øker til 13 % ved et epidemisk utbrudd (3). Spesielt utsatt er kvinner med barn i skolealder, lærere og førskolelærere, noe som gjenspeiles i våre kasuistikker. I Danmark ble det påvist 50 % serokonversjon hos kvinner som hadde ett eller flere barn med infeksjon.
Infeksjon i svangerskapet
Dersom en gravid smittes, er risikoen for fosterinfeksjon 33 % (4). Infeksjonen kan hos fosteret være selvbegrensende eller få alvorlige følger. Risikoen for alvorlige manifestasjoner er 3 – 24 % (5 – 7), mens risikoen for fosterdød angis til 5 – 14 % (1, 8, 9), og er hyppigst i svangerskapsuke 9 – 16 (4). Hydrops påvises 2 – 17 uker etter mors primærinfeksjon, mens fosterdød oftest inntrer omkring åtte uker etter eksposisjon (7, 8,). Ved føtal hydrops er dødeligheten ca. 50 %, men ved behandling med intrauterine transfusjoner kan denne reduseres betydelig (1, 5). I tredje trimester er fosterdød som følge av parvovirus B19-infeksjon ofte ikke ledsaget av hydrops (8). Parvovirus B19 er anført som den vanligste kjente virale årsak til fosterdød, 5 – 10 % (8).
Det er ikke vist at parvovirus B19 er teratogent for mennesket. Oppfølging av barn som var infisert i fosterlivet, men som overlevde med eller uten behandling, tyder på at de har gode utsikter (4, 10).
Sykdomsmekanismer ved infeksjon hos fosteret
Viruset bindes til en spesifikk glykosidreseptor, erytrocytt P-antigen, i erytropoetiske celler. Men antigenet finnes også i megakaryocytter, endotelceller, placenta, føtal lever og myokard, noe som forklarer det føtale sykdomsbildet også hos våre pasienter (5, 11).
Fosteret er mest sårbart for følger av infeksjonen i 2. trimester (12, 13). Da er de erytropoetiske cellenes levetid kort, og behovet for nye erytrocytter raskt økende. Dette faller sammen med den hepatiske perioden med hematopoetisk aktivitet (5, 9).
Hydrops er et resultat av anemi og hypoksi, hjertesvikt og leveraffeksjon med lav albuminkonsentrasjon. En sjelden gang blir infeksjon i fosterlivet persisterende, og barna må følges opp etter fødselen med blodtransfusjoner og immunglobulin.
Diagnose, oppfølging og behandling
Siden tilstanden kan behandles, bør det ved kjent eller mistenkt eksposisjon utføres serologisk diagnostikk av gravide kvinner. Deteksjonsraten med denne metoden er 81,3 % (14, 15). Dersom IgM-antistoff mot parvovirus B19 påvises, er dette tilstrekkelig grunnlag for henvisning til spesialavdeling. I føtalt blod er sensitiviteten av serologiske undersøkelser lav (43,8 %). Dopplermålinger i fosterhjerne, hjerte, ductus venosus, umbilikalvene og -arterie gir en oversikt over fosterets sirkulatoriske situasjon og kan avdekke anemi (16, 17), myokardaffeksjon og portahypertensjon (18). Påvisning av parvovirus B19-DNA med polymerasekjedereaksjon er en sensitiv metode og kan utføres i mors blod, fostervann, placenta eller navleveneblod. På grunn av risiko for komplikasjoner vil kordocentese vanligvis bare bli gjort i tilfeller der det er berettiget mistanke om anemi.
I de tilfellene der mor er smittet, men hvor det ennå ikke er symptomer hos fosteret, vil gjentatte dopplerundersøkelser kunne indikere lavt hemoglobinnivå før hydrops utvikles.
Studier tyder på at omtrent en tredel av tilfellene av føtal hydrops helbredes spontant, mens 84 % av fostre med hydrops som blir behandlet med transfusjoner, overlever (7, 19). Gjentatte transfusjoner kan være nødvendig.
Den gunstige effekten av immunglobulin til barn og voksne med underliggende anemier eller med svekket immunforsvar er ikke beskrevet hos gravide eller hos fostre (20).
Vaksine er under utvikling, men det er uklart om kvinner i fertil alder er kandidater for slik profylakse.
Man har ikke funnet argumenter for å gjennomføre screening av risikobefolkningen (2), men det antas at økt bevissthet om infeksjonen og dens følger er en viktig strategi for å få leger til å rekvirere serologisk diagnostikk av rett gruppe pasienter.
Oppsummering
Gravide som eksponeres for smitte eller får symptomer på infeksjon, bør undersøkes med serologiske prøver for påvisning av IgM- og IgG-antistoff mot parvovirus B19. Dersom den gravide er mottakelig for smitte, bør prøvene gjentas 2 – 3 uker senere.
Hvis spesifikt IgM-antistoff påvises, bør kvinnen henvises til en spesialavdeling som kan følge fosteret med ultralyd- og dopplerundersøkelser for å avdekke en behandlingstrengende fosteranemi.
Diagnostikk med henblikk på parvovirus B19-infeksjon bør inngå i rutinene ved intrauterin fosterdød.