Akutt høyfebril sykdom byr på betydelige diagnostiske utfordringer, spesielt når pasienten har svekket allmenntilstand og er systemisk påvirket. Vi presenterer en pasient med akutt innsettende systemiske symptomer og tegn, men der infeksjonsfokus var vanskelig å oppdage.
En 17 år gammel jente med behov for øyeblikkelig hjelp ble henvist til akuttmottaket, Sørlandet Sykehus Kristiansand etter å ha vært febersyk i to-tre dager. Legevaktlegen hadde ved to anledninger dagen før innleggelsen ikke sett nødvendigheten av å gjøre en nærmere utredning av hennes febersykdom. Før hun henvendte seg til legevakten, hadde hun vært i god form og blant annet dratt på turer til badestranden.
Ved innleggelsen kom det frem at hun hadde tiltakende feberfølelse, selvmålt til 40,5 °C aksillært, med flere korte frostanfall. I tillegg klagde hun over frontal, trykkende hodepine. Tidligere samme dag hadde hun én enkeltstående vandig avføring. Hun var elev på videregående skole, brukte ingen medisiner, ingen tobakk og var tidligere frisk. Hun bekreftet pågående menstruasjonsblødning, men brukte ikke tampong.
Klinisk undersøkelse avdekket en medtatt 17-årig jente som lå stille i sengen, sammenkrøket og til dels sovende. Hun reagerte på tiltale og lot seg motvillig kommandere til undersøkelser. Undersøkelsen avdekket varm og tørr hud, uanstrengt respirasjon, ingen cyanose og god perifer sirkulasjon. Blodtrykk 115/70 mm Hg, puls 130 slag per minutt, temperatur 39,5 °C i øret. Man fant ingen nakkestivhet, og hodepinen ble ikke forverret ved nakkeundersøkelser. Både Königs test og Brudzinskis test var negativ. Over symfysen fant man en centimeterstor palpabel tumor i hudnivå, ruborøs, varm og smertefull ved palpasjon, men uten sekresjon og med intakt hudbarriere (fig 1). Den hadde lokalt erytem i et område på 3 x 3 cm. Tumoren hadde oppstått uker i forveien, men hun husket ingen penetrerende objekter eller hudsår. Det var ingen andre hudmanifestasjoner.
Klinisk-kjemiske prøver ved innkomst omfattet CRP 161 mg/l, leukocytter 8,2 g/l med nøytrofil dominans på 7,9 g/l, bilirubin 33 µmol/l, ALAT 82 U/l, INR 1,5, kreatinin 93 µmol/l, s-natrium 130 mmol/l og p-kalium 3,3 mmol/l. Lumbalpunksjon ved innkomst viste klar spinalvæske, trykk 18 cm vann, 3 leukocytter og totalprotein 35 l (150 – 500 mg/l).
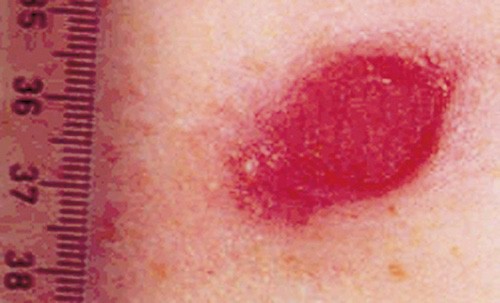
Figur 1 Bilde av kutan abscess på bukens fremside
Funnet på buken ble oppfattet som en lokal abscess. Det var imidlertid vanskelig å bedømme abscessens dybde ved klinisk undersøkelse, mest på grunn av smerter som ble utløst ved palpasjon. På bakgrunn av mistanke om abscessog oppfyllelse av to kriterier for systemisk inflammatorisk responssyndrom, startet man med antibiotika umiddelbart etter blodkulturer og spinalpunksjon. Antibiotikavalget ble gjort ut fra mistanke om sepsis med utgangspunkt fra abdomen, da man ikke kunne verifisere abscessens dybde. Opplysningen om vanntynn avføring ble også tatt med i denne vurderingen. Hun fikk derfor trippelregime med ampicillin, tobramycin og metronidazol.
Ultralyd abdomen viste en 6 x 10 x 10 mm stor væskeholdig abscess i hudnivå, uten kommunikasjon med dypere lag eller fri bukhule (fig 2). Denne ble åpnet ved punksjon, og 0,5 ml purulent abscessinnhold ble sendt til gramfarging og mikroskopi samt dyrking. En gynekologisk undersøkelse avdekket normale forhold i vagina, portio og vulva. Ingen tampong ble funnet.
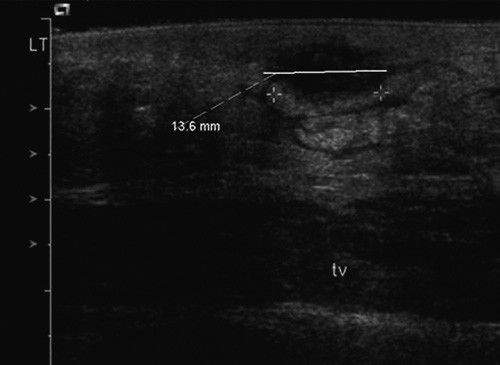
Figur 2 Ultralyd av nedre abdominalvegg: Uregelmessig lavekkogen lesjon beliggende 3 mm subkutant, ca. 14 mm i største diameter. Det er generelt subkutant ødem i området
Sent i 1970-årene fant man i epidemiologiske undersøkelser fra USA en sammenheng mellom bruk av tampong og utvikling av alvorlig infeksjonssykdom. Spesielt hyppig ble dette sett hos yngre menstruerende, kaukasiske kvinner (1).
Seks timer etter innkomst forverret sykdomsbildet seg. Blodtrykket falt fra 110/55 mm Hg til 90/50 mm Hg og lå deretter vedvarende lavt omkring 90/40 mm Hg. Temperatur intravesikalt ble målt til 39,7 °C. Hjertefrekvensen var 110 slag per minutt, men steg raskt til 140 – 150 slag per minutt. Væsketerapi pågikk fortløpende, og pasienten var på dette tidspunktet rehydrert med 3 000 ml klare væsker for å opprettholde blodtrykket. Imidlertid måtte vi intensivere væsketerapien da tilstanden ble ytterligere komplisert, med manglende blodtrykksrespons på væskebehandling og tegn på hypoksisk respirasjonssvikt. Blodgass viste pH 7,39, pCO₂ 3,7 kPa, pO₂ 10,3 kPa, baseoverskudd –7,2 mmol/l, bikarbonat 16,8 mmol/l og laktat 3,0 mmol/l, stigende til 4,1 – 7,7 – 10,1 mmol/l. Respirasjonen endret karakter fra uanstrengt til forsert. Røntgen thorax viste utbredte lungefortetninger bilateralt. CT thorax avdekket konfluerende forandringer i alle lungeavsnitt forenlig med alveolært ødem og noe pleuravæske bilateralt. CT abdomen viste ingen åpenbare tegn til intraabdominal patologi, men noe væske ble sett omkring lever, milt og i det lille bekken. Pasienten ble pressoravhengig med noradrenalin, dopamin og adrenalin og respiratortrengende fra time sju etter innkomst. De 16 første timene fikk hun tilført 9 000 ml klare væsker.
Differensialdiagnostisk finnes relativt få tilstander med sjokkutvikling hos unge tidligere friske individer: Sepsis, bakteriell meningitt, toksisk sjokk-syndrom, og dersom reiseanamnese: denguefeber, malaria og tyfoidfeber. Med det angitte CT-funnet og det dramatiske forløpet var det indikasjon for diagnostisk laparotomi på vitalt grunnlag ettersom infeksjonsfokus tilsynelatende manglet. 2 dl klar bukvæske ble avdekket. Normale, vitale forhold ble påpekt omkring intra- og ekstraperitoneale organer i abdomen.
Neste morgen, 12 timer etter innkomst, var pasienten sirkulatorisk stabil på respirator med delvis uttrapping av pressorstøtte, unntatt noradrenalin. CRP ble målt til 292mg/l, og det var akseptable blodgasseverdier, men fortsatt høyt laktatnivå (9,1 mmol/l). Røntgeninfiltrater på lungene var i regress, men det var fortsatt eksessiv pleuravæske bilateralt. Av mikrobiologiske prøver kunne man bekrefte grampositive kokker i hauger fra kutan abscess på buken samt granulocytter i bukvæsken. Antibiotika ble byttet til kloksacillin og tazobaktam + piperacillin.
Etter at både sirkulatorisk og til dels respiratorisk kollaps ble korrigert, så man bedring på alle områder. Pasienten ble ekstubert fra respirator etter ca. 26 timer. Senere var hun hemodynamisk stabil uten pressorstøtte med middels arterietrykk (MAP) omkring 100 mm Hg og hjertefrekvens omkring 90 slag per minutt. Saturasjonen stabiliserte seg på omkring 98 %. Hun ble afebril ca. 48 timer etter innleggelse, og CRP < 10 mg/l ble sett etter seks døgn. Tazobaktam + piperacillin ble gitt i totalt to døgn parallelt med kloksacillin som ble gitt intravenøst i ti dager. Utskrivning fant sted etter 11 døgn. Diagnosene lød: septisk sjokk, sepsis med gule stafylokokker, disseminert intravaskulær koagulasjon, akutt lungesvikt-syndrom og kutan abscess. En peroral kur med kloksacillin ble gitt i sju døgn etter utskrivning. Ved sårkontroll ca. to uker etter utskrivning fant man ved inspeksjon skjelling av hud (deskvamasjon), spesielt i håndflater og fotsåler.
Bakterieundersøkelser av kutan abscess viste rikelig vekst av Staphylococcus aureus i renkultur. Ingen resistensproblematikk utover penicillinasedanning i stafylokokkene ble påvist. Bakterieundersøkelser av spinalvæske, blodkultur, bronkialsekret, urinkultur, avføring og bukvæske var alle uten vekst. Man kunne ikke titrere serumnivå av anti-stafylokokk-antistoff i prøve tatt på dag 5. St. Olavs Hospital analyserte stafylokokkene og fant genmateriale forenlig med produksjon av stafylokokker med eksfoliativt toksin B (ETB). Åtte dager etter innleggelse ble det bekreftet fra referanselaboratoriet i København at stafylokokkene også inneholdt gen for toksisk sjokk-syndrom toksin-1 (TSST-1). Stafylokokker har relativ stor evne til toksinproduksjon (2). Det er også bekreftet at multiple stafylokokktoksiner i dyremodeller potenserer effekten av hverandre på en synergistisk måte, spesielt ved tampongassosiert toksisk sjokk-syndrom (3).
Diskusjon
Denne dramatiske sykehistorien har altså sitt utgangspunkt i en centimeterstor kutan abscess (karbunkel) forårsaket av toksinproduserende gule stafylokokker. Vi lyktes ikke i å avdekke et større eller annet infeksjonsfokus, noe vi hadde ventet ut fra det kliniske bildet. Historien illustrerer et fulminant toksisk sjokk-syndrom fra en relativ banal infeksjon hos en ellers frisk ungdom. Pasienten oppfylte fem av seks kriterier for toksisk sjokk-syndrom etter diagnosekriterier utarbeidet av Centers for Disease Control and Prevention (4): Feber, hypotensjon, multiorganfunn, negative funn ved annen dyrking eller serologi, og huddeskvamasjon. Hun manglet karakteristisk erytrodermi ved innkomst. Huddeskvamasjon ses vanligvis 1 – 2 uker etter symptomdebut, men kan utebli (5).
Det er avgjørende å gjøre kirurgisk intervensjon i operable fokus ved mistanke om toksinmediert stafylokokksykdom. Fremmedmaterialer som tampong og spiral må fjernes, sårinfeksjoner må revideres, abscesser må dreneres og dype infeksjoner må eksploreres. Vår pasient fikk bred antibiotisk dekning med piperacillin + tazobaktam i kombinasjon med kloksacillin. Dette ble foreskrevet i den hensikt å dekke eventuell multimikrobiell flora som ved intraabdominal infeksjon. Baktericide midler som betalaktamasestabilt penicillin er veldokumentert både som eradikeringsterapi og residivprofylakse ved toksisk sjokk-syndrom, men forårsaker sannsynligvis økning av serum-TSST-1 på grunn av bakteriolyse. Imidlertid er proteinsyntesehemmer som klindamycin veldokumentert med serum-TSST-1-reduksjon med inntil 90 % (6). Immunoglobuliner har liten plass i behandlingen av toksisk sjokk-syndrom, men anbefales ved immunopatier og behandlingsrefraktær toksisk sjokk-syndrom. Sannsynligvis har immunoglobuliner bedre effekt når syndromet er forårsaket av streptokokker enn stafylokokker (7). Kortikosteroider er forbundet med mildere forløp og raskere feberfrihet (8).
Det er vanlig å inndele toksisk sjokk-syndrom forårsaket av stafylokokker i mentruasjonsassosierte og ikke-menstruasjonsassosierte tilfeller. Mens insidens og letalitet har vært jevnt synkende blant menstruasjonsassosierte tilfeller, ser man en relativ høy og stabil letalitet på omtrent 5 % vedikke-menstruasjonsassosierte tilfeller i USA (1). Prevalensundersøkelser viser at ca. 80 % av friske tenåringer har antistoffer mot TSST-1. Pasienter som utvikler toksisk sjokk-syndrom av stafylokokker mangler TSST-1-antistoffer. Residiverende toksisk sjokk-syndrom er også beskrevet. Hos alle disse pasientene finner man ingen eller defekt produksjon av TSST-1-antistoffer (9). Pasienten vår er foreløpig ikke testet for serokonvertering. Spesifikk TSST-1-antistoffterapi er utforsket på musemodeller og har der vist effekt på letalitet, men er ikke testet i kliniske forsøk på mennesker. Immunmodulerende terapi med pentoksyfyllin, et hemoreologisk middel som øker muskelblodstrøm ved perifer oblitererende aterosklerose, har vist seg å blokkere TSST-1-mediert og ETB-mediert leukocyttfrigjøring av tumornekrosefaktor-α ved toksisk sjokk-syndrom. Pentoksyfyllin beskytter dermed mot superantigener (10).