Sommeren og høsten 2009 var det en påfallende treg epidemiutvikling for pandemisk influensa A(H1N1)-virus. Vi tror at interferens med andre respiratoriske virus, spesielt rhinovirus, kan ha bidratt til dette. Interferenshypotesen ble lansert av en av oss i 1982. Muligens er interferensfenomener vanlige i utbruddsutviklingen for epidemiske virus. Hvis så er tilfellet, er cytokinene, kanskje spesielt interferon, de mest sannsynlige utøvere av denne effekten.
I slutten av april 2009 ble det i Nord-Amerika påvist et nytt influensa A(H1N1)-virus. Dette nye viruset hadde flest genetiske elementer fra svin. Det var en rask spredning over mesteparten av kloden. 11. juni erklærte WHO den første influensapandemien siden hongkongsyken i 1968.
Influensaepidemiologi
I Norge ble de første tilfellene påvist i midten av mai 2009. De følgende ukene var det som forventet en økning i antall laboratoriebekreftede tilfeller av det nye viruset samt en tilsvarende økning i andelen som fikk diagnosen influensaliknende sykdom (ILS) ved besøk hos allmennlegen. Imidlertid, fra annen halvdel av juli, dvs. uke 30, observerte man en uventet nedgang i antall laboratoriebekreftede tilfeller. Dette til tross for at man ikke så samme reduksjon i andelen pasienter med diagnosen influensaliknende sykdom. Dette vedvarte til medio oktober (uke 42), da det var en rask økning i antall influensaviruspåvisninger samt økt andel av pasienter med influensaliknende sykdom. Utbruddet kulminerte primo november (uke 45), og fra årsskiftet var man tilbake på ikke-epidemisk nivå (fig 1) (1).
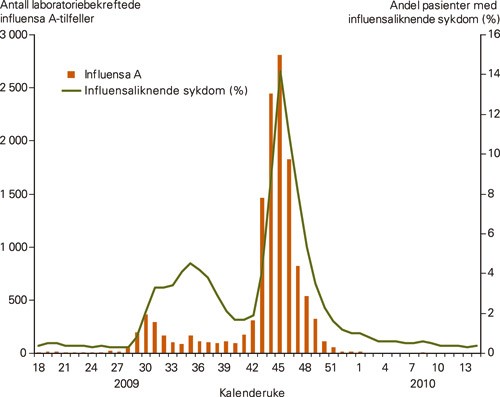
Figur 1 Antall laboratoriebekreftede tilfeller av influensa A-virus fra uke 18 i 2009 til uke 14 i 2010 i Norge samt andelen legekonsultasjoner som førte til den kliniske diagnosen «influensaliknende sykdom» (1)
Rhinovirusinterferens?
I Sverige var epidemiutviklingen nesten identisk med den man så i Norge. Annika Linde og medarbeidere sendte høsten 2009 en forespørsel til svenske mikrobiologiske laboratorier om hvilke andre respiratoriske virus man kunne påvise i de negative influensaprøvene. Svaret var unisont: Rhinovirus dominerte. Det var også sporadiske funn av andre respiratoriske virus som enterovirus og adenovirus. Nøyere undersøkelser viste at nedgangen i andelen positive influensaprøver falt sammen med den tilsvarende økningen av andelen diagnostiserte rhinovirusinfeksjoner. Kunne den store rhinovirusaktiviteten sensommeren og høsten 2009 ha hemmet epidemiutviklingen for pandemisk influensa A(H1N1)-virus i Sverige (2)?
Norske forhold
I Norge har man ved St. Olavs hospital i Trondheim i en årrekke inkludert rhinovirus i testpanelet ved luftveisprøver fra sykehusinnlagte barn. I perioden 2007 – 09 var det en økning i antall diagnostiserte rhinovirusinfeksjoner fra midtsommers og utover høsten (3).
Frankrike
I Lyon registrerte forskere i vintersesongene 2008 – 09 og 2009 – 10 en tidlig start på rhinovirusutbruddene. I begge sesongene ble disse etterfulgt av distinkte utbrudd med respiratorisk syncytialvirus (RSV) og influensavirus. I 2008 – 09 kom RSV-utbruddet før influensaen, i siste sesong kom influensautbruddet først (4).
Virus
I likhet med mange andre respiratoriske virus er influensavirus komplekst oppbygd, med en lipidmembran som danner den ytre kappen. Slike virus er sårbare og skades lett dersom de ytre forholdene er ugunstige. Studier har vist at membranen er mest stabil i tørt og kjølig vær (5). Dette forklarer kanskje hvorfor influensavirus og andre kappekledde respiratoriske virus som respiratorisk syncytialvirus og parainfluensavirus vanligvis har størst aktivitet i vintermånedene. Sammenliknet med influensavirus er rhinovirus enkelt oppbygd. Selve viruspartikkelen består av et ytre kapsid (skall) som omslutter nukleinsyren. Under ugunstige værforhold vil rhinovirus ha klare fortrinn fremfor influensavirus og andre komplekst oppbygde respiratoriske virus (3). Figur 2 illustrerer oppbygningen av henholdsvis rhinovirus og influensavirus.
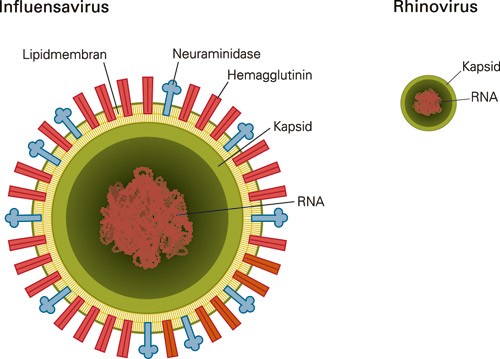
Figur 2 Et rhinovirus er et lite picornavirus (28 – 30 nm) som består av viralt RNA omgitt av et ytre kapsid (skall). Influensavirus er et betydelig større RNA-virus (90 – 120 nm). Utenpå kapsidet er det en ytre lipidkappe som danner feste for viktige strukturer som hemagglutinin og neuraminidase (1 nm er 1/1 000 000 mm)
Dersom interferensteorien er korrekt, kan rhinovirus kanskje ha funnet sin nisje sensommer og høst og har således kunnet leve i fred og fordragelighet med eventuelle konkurrerende virus. Hva så hvis det plutselig dukker opp et nytt virus som ennå ikke har funnet sin plass i hierarkiet og opptrer på tvers av disse årstidsfasene? Da vil sannsynligvis interferenskreftene slå til – og resultatet vil bli forsinket epidemiutvikling for inntrengeren (3). I denne sammenheng vil vi nevne en studie av Greer og medarbeidere (6). De registrerte at mennesker som nylig hadde gjennomgått en rhinovirusinfeksjon, var lite mottakelige for andre respiratoriske virus.
Er det rimelig at noen små og unnselige rhinovirus skal kunne hemme og delvis stoppe epidemiutviklingen for et nytt pandemisk influensavirus? Hvis det er tilfellet, har rhinovirus, i tillegg til sin enkle oppbygning, enda en fordel – nemlig det store antall serotyper. Man kjenner mer enn 100 forskjellige rhinovirustyper som ikke gir noen innbyrdes serologisk kryssbeskyttelse. De fleste mennesker gjennomgår flere rhinovirusinfeksjoner hvert år, mens det kan gå flere år mellom hver gang man pådrar seg infeksjon med andre luftveisvirus, f.eks. influensavirus.
Virusinterferensteorien – en gammel tanke
Basert på norske observasjoner ble interferensteorien fremsatt i 1982 (7). Bakgrunnen var at i vintre hvor RSV-utbruddene startet før influensasesongen, kulminerte disse utbruddene idet influensautbruddene startet. Tilsvarende, dersom RSV-utbruddene ikke hadde nådd epidemisk nivå før influensaen kom, fikk man små RSV-utbrudd uten noen tydelig topp. Senere undersøkelser har understøttet disse funnene (8, 9), men de er ikke entydige (10).
Det kan synes uvant å snakke om interferens i utbruddsutviklingen for epidemiske virus. Imidlertid er det velkjent at dersom man blander sammen forskjellige virus i cellekulturer, vil det oppstå interferensfenomener som gir seg til kjenne ved at kulturene får redusert mottakelighet for det sist tilsatte viruset. Det var studier av disse fenomenene som førte til at Isaacs & Lindenmann i 1957 oppdaget interferon (11), en innsats som ble belønnet med nobelprisen i fysiologi eller medisin.
Det er egentlig usannsynlig at disse fenomenene kun skal gjøre seg gjeldende in vitro og ikke in vivo (8). Alle levende organismer er jo omfattet av Darwins utviklingslære, hvor naturlig seleksjon og alles kamp mot alle er sentrale begreper. For å spissformulere – det er usannsynlig at epidemiske virus skal kunne sirkulere helt fritt og uavhengig av hverandre. I så fall vil det være i strid med helt sentrale elementer i utviklingslæren. Spørsmålsstillingen må vel heller være: Er de aktuelle virus i en slik innbyrdes posisjon at interferenskreftene blir eksponert, og er våre overvåkingssystemer gode nok til å fange dem opp? Annika Linde og medarbeidere avslutter sin artikkel med å foreslå at influensaepidemiologien også bør relateres til andre respiratoriske virus for å bedre forståelsen av den virkelige epidemiologiske situasjonen. Likeledes bør respiratoriske virus overvåkes gjennom hele året for at man skal ha pålitelig bakgrunnsinformasjon om influensaliknende sykdom og akutte respiratoriske infeksjoner. Dette er viktig når et pandemisk virus som ikke følger det vanlige spredningsmønsteret opptrer (2). Vi støtter disse synspunktene.
Selv om virusinterferensteorien fortsatt er en ren hypotese, gir den en meget plausibel forklaring på hvorfor for eksempel spanskesyken og andre pandemier – i motsetning til vanlig sesonginfluensa – har tendens til å opptre i bølger.
Virus er som oss andre
Virus mangler egenmetabolisme. De har kun evnen til, via sin nukleinsyre, å tvinge vertscellen til å produsere nye viruspartikler. Virus anses derfor av mange å representere et grenseområde mellom levende og dødt materiale. På mange vis kan interferensteorien forandre på dette bildet – vi ser konturene av trekk som gjenkjennes hos høyerestående organismer, inklusive Homo sapiens. Under normale forhold «lever» epidemiske virus stort sett i fordragelig sameksistens med hverandre, men i likhet med mange andre er de «intrigerende» og «misunnelige». Dette kommer tydelig frem dersom en nykomling forsøker å forlate sin tiltenkte plass i køen og snike seg til en plass lenger fremme.
Interferon
Hvordan skal man forklare interferensfenomenene? I en rekke artikler fremheves det at cytokinene, særlig interferon, er de sannsynlige utøvere av denne effekten (2, 6 – 9, 12). Interferon inngår i kroppens førstelinjeforsvarsverk og er en del av det medfødte immunapparatet. Interferonets virkningsmekanisme er kort fortalt at virusinfiserte celler produserer et lavmolekylært protein (interferon) som diffunderer ut av cellen og beskytter ikke-infiserte naboceller mot angrep fra det angjeldende virus. I motsetning til det ervervede immunapparat, med sine antistoffer, er kjennetegnet ved interferon at virkningen ikke er virusspesifikk. Det vil si at i tiden like etter en infeksjon med f.eks. rhinovirus eller influensavirus vil man være i en «antiviral» fase hvor man er mer eller mindre beskyttet mot nye virusinfeksjoner (2, 6, 12). Under en virusepidemi vil derfor andelen individer som er mottakelige overfor andre virus avta. At det aktuelle virus bruker denne effekten for å holde konkurrerende virus unna matfatet, er i så fall et genialt trekk. Hvem er egenlig den smarteste, viruset eller verten?