En 25 år gammel kvinne, sykmeldt i ett år for ryggsmerter, hadde i perioder merket moderate høyresidige abdominalsmerter. Hun var for øvrig frisk, brukte ikke narkotika, men drakk alkohol på fest i helgene. To uker før det aktuelle ble hun innlagt med magesmerter etter inntak av alkohol. På mistanke om appendisitt ble det gjort eksplorativ laparoskopi med normale funn. Hun var etterpå plaget med kvalme og moderate magesmerter. Hun drakk igjen alkohol dagen før den aktuelle innleggelsen i gastrokirurgisk avdeling med smerter oppad i abdomen med utstråling til rygg og dels til fossa iliaca. Hun var tungpusten ved innkomst og fikk oksygen.
Kraftige anfall med magesmerter i øvre og sentrale deler av abdomen ledsaget av kvalme kan gi mistanke om blant annet akutt appendisitt, ulcussykdom og gallestein. Sammenheng med alkoholinntak gjør akutt pankreatitt til en mulig differensialdiagnose selv hos en ung, frisk kvinne. Hun var nylig laparoskopert uten tegn til appendisitt og hun ble i første omgang satt opp til gastroskopi neste dag på grunn av mistanke om ulcussykdom. Ultralyd abdomen ble rekvirert med tanke på gallestein.
Ultralyd abdomen viste normale forhold. Ved gastroskopi neste dag fikk hun en akutt reaksjon med brystsmerter og stridor idet skopet ble trukket opp fra en normalt utseende ventrikkel. Dette ble oppfattet som en anafylaktisk reaksjon og pasienten fikk adrenalin, hydrokortison og antihistamin intravenøst. Ved overflytting til overvåkingsavdeling var hun blek, klam, hypotensiv med lett stridor og takypné, men ikke takykardi. Fortsatt hadde hun sterke magesmerter. Blodkulturer ble tatt og antibiotika gitt pga. mistanke om sepsis.
Den akutte reaksjonen på gastroskopiundersøkelsen ble først oppfattet som en anafylaktisk reaksjon. Pasienten hadde kun fått lidokainspray som lokalbedøvelse i forbindelse med skopien. Anafylaksiberedskap skal alltid være en del av forberedelsene til skopiundersøkelser. Iatrogen ruptur/skade av oesophagus eller trachea er sjelden, men må alltid vurderes som årsak til akutte komplikasjoner til øvre skopier. CT thorax inngår i utredningen av slike situasjoner.
Røntgen thorax og CT thorax med lungeemboliprotokoll var normale. Ekkokardiografi ble gjort med tanke på mulig aortadisseksjon, men undersøkelsen viste normale forhold. CT abdomen viste kun litt ødem rundt galleblæren samt litt væske i abdomen. Gynekologisk undersøkelse var normal. EKG viste uspesifikke ST-segmentforandringer. Blodprøver viste pO₂(a) 8,9 kPa, pCO₂(a) 5,1 kPa, pH 7,37, aktuell bikarbonat 21,5 mmol/l, baseoverskudd –3,4 mmol/l, CRP 11 mg/l, pancreasamylase 770 U/l (referanseområde 20 – 100 U/l) (fig 1), troponin T 0,7 &181;g/l, CK 157 U/l og CK-MB 21 U/l. Øvrige blodprøver var normale. Serologiske tester for HIV og Legionella samt immunologiske prøver inkludert antinukleære antistoffer (ANA) var negative. Direkte mikroskopi og undersøkelse med polymerasekjedereaksjon gav ikke holdepunkt for tuberkulose. Dag 3 fikk pasienten kvalme og økende abdominalsmerter. Hun satt fremoverlent i sengen med flekterte knær og ble økende dyspneisk og takypneisk med frekvens på 50/min. pO₂(a) sank til 7,9 kPa til tross for oksygentilførsel. Hun ble sedert og tilkoblet respirator, og ventrikkelsonde ble nedlagt. Røntgen thorax viste nytilkomne bilaterale, diffuse, flekkvise fortetninger (fig 2). Temperaturen var nå 39,5 °C. Blodprøver viste pancreasamylasestigning til 1400 U/l. CRP var 20 mg/l og albumin 24 g/l. Tilstanden ble oppfattet som akutt pankreatitt med lungekomplikasjoner forenlig med sjokklunge.

Serumnivå av pancreasamylase og lipase i enheter/liter (U/l) hos 25 år gammel kvinne innlagt med magesmerter og respirasjonssvikt. Referanseområde pancreasamylase 20 – 100 U/l, lipase 20 – 160 U/l
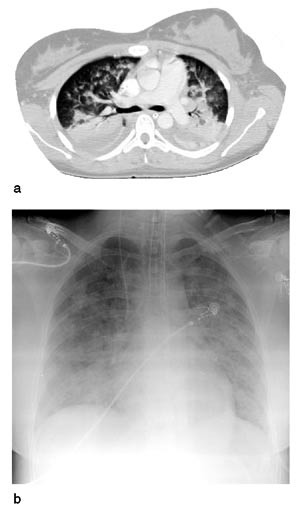
Figur 2 Lungebilder tatt fire dager etter innkomst. a) CT thorax: utbredte, flekkvise parenkymfortetninger, basal atelektase med antydet luftbronkogram og pleuravæske bilateralt. b) Røntgen thorax: utbredte, ulne, flekkvise dels konfluerende fortetninger i begge lunger
Akutte magesmerter med pancreasamylasestigning gav tidlig mistanke om affeksjon av pancreas. Det kliniske bildet ved akutt pankreatitt domineres av smerter lokalisert til epigastriet og området rundt umbilicus med utstråling til rygg, bryst og flankeregioner, ofte ledsaget av kvalme og oppkast. Typiske funn er subfebrilia, takykardi, hypotensjon og eventuelt sirkulatorisk sjokk ved alvorligere former. Vår pasient hadde typiske symptomer og funn bortsett fra manglende takykardi. Imidlertid var hun svært medtatt og med lungekomplikasjoner som medførte behov for respiratorbehandling. Et slikt alvorlig bilde uten påvisbare pancreasforandringer på CT gjorde det viktig å utrede alternative differensialdiagnoser, f.eks. sepsis med utgangspunkt i abdomen inkludert iskemisk tarm. Nedsvelging av narkotiske stoffer som amfetamin og kokain ble vurdert som en differensialdiagnose, men fravær av takykardi gjorde dette mindre sannsynlig. Pasientens lungesymptomer var forenlig med utvikling av sjokklunge (engelsk: acute respiratory distress syndrome, ARDS). Det typiske bildet ved sjokklunge er dyspné, takypné og hypoksemi med synkende pO₂(a) til tross for adekvat tilførsel av oksygen samt bilaterale diffuse lungefortetninger som ikke skyldes hjertesvikt. Det er viktig å utelukke andre årsaker til akutt respirasjonssvikt som f.eks. lungeemboli og pneumoni. Tilstanden må identifiseres raskt og behandlingen vil som regel inkludere assistert ventilasjon med respirator.
Dag 4 tilkom utbredte bilaterale fortetninger forenlig med ødem/eksudat også på CT thorax (fig 2). CT abdomen ble gjentatt, men viste uendrede funn med fortsatt normalt utseende pancreas (fig 3). For å utelukke andre patologiske forhold ble pasienten laparoskopert med normale funn i abdomen og bekken. Hun var nå afebril og det ble ikke påvist vekst av mikrober verken i blod, abdominalvæske eller trakeal-/cervixsekret. Amfetamin, kokain og cannabinoider ble ikke påvist verken i urin eller blod.

Figur 3 CT abdomen viser en normal pancreas
Rundt 25 % av tilfellene av akutt pankreatitt progredierer til alvorlig pankreatitt ledsaget av komplikasjoner (1). Lokale komplikasjoner omfatter intra- eller peripankreatisk eksudat, nekrose, blødning, infeksjon, abscess, utvikling av pseudocyste samt affeksjon av nærliggende organer. Systemiske komplikasjoner involverer hyppigst det kardiovaskulære system, lungene, nyrene og blodet. I tillegg kommer metabolske komplikasjoner som hyperglykemi, hypokalsemi og hypertriglyseridemi. Ofte utvikles multiorgansvikt som domineres av kardiovaskulær affeksjon med hypotensjon og sjokk, lungesvikt, akutt nyresvikt og disseminert intravaskulær koagulasjon (DIC). Kardial affeksjon medfører av og til uspesifikke ST-T-forandringer på EKG, slik vår pasient hadde, og som kan simulere myokardiskemi. Pasienten hadde dessuten et lite utslipp av hjerteenzymer som vi oppfattet som uttrykk for en uspesifikk myokardaffeksjon. Dette er noe vi ofte ser hos intensivpasienter. Hjerteinfarkt er beskrevet som komplikasjon til akutt pankreatitt (1), men dette forekommer svært sjelden.
Dag 5 viste røntgen thorax betydelig tilbakegang av lungefortetningene. Dag 6 ble pasienten ekstubert, men hun var fortsatt sløv og medtatt de neste dagene. MR caput viste normale forhold. MR pancreas og magnetisk resonanskolangiopankreatikografi (MRCP) tatt før avreise (dag 15) viste normale forhold. Pasienten fikk etter hvert tilbake magesmerter, men i svært moderat grad. Hun fikk beskjed om avhold fra alkohol. Ved kontroll etter seks uker var blodprøvene inkludert pancreasamylase og lipase nærmest normalisert. Pasienten var i god allmenntilstand, men fortsatt plaget med konstante smerter av moderat karakter i epigastriet. Til tross for normale forhold ved pancreas både ved CT- og MR-undersøkelser opprettholdes diagnosen pankreatitt med komplikasjoner i form av respirasjonssvikt.
Uttalte systemkomplikasjoner er vanligvis forbundet med akutt og alvorlig nekrotiserende pankreatitt. Vår pasient illustrerer at slike komplikasjoner også kan oppstå ved mildere former for akutt pankreatitt uten påvisbare forandringer på CT-undersøkelser og med kun moderat stigning i serumnivået av pancreasenzymer.
Diskusjon
Akutt pankreatitt forekommer relativt hyppig med en årlig insidens på 5 – 50 per 100 000 innbyggere. Akutt pankreatitt varierer fra milde former med pancreasødem til nekrotiserende former med betydelige lokale og systemiske komplikasjoner. Dødeligheten er 6 – 10 % ved mild pankreatitt og øker til rundt 30 % ved alvorlig pankreatitt (2 – 4). Vanligste årsaker til pankreatitt er gallestein (ca. 45 %), bruk av alkohol (ca. 35 %), hypertriglyseridemi, virusinfeksjoner, medikamentbruk (1) samt komplikasjoner etter endoskopisk retrograd kolangiopankreatikografi (ERCP) og kirurgi.
Forhøyet konsentrasjon av amylase i serum gir vanligvis diagnosen. Ofte bestemmes pancreasamylase (pancreasspesifikt isoenzym) for å utelukke amylase fra andre organer. Nivået av totalamylase i serum faller ofte etter 2 – 4 døgn, mens nivået for lipase først normaliseres etter 1 – 2 uker. Lipase er derfor en sikrere test enn amylase i diagnostikken (5). Vår pasient hadde et typisk fall i pancreasamylasenivå etter fire døgn, mens lipasenivået holdt seg vedvarende høyt (fig 1). I tillegg hadde pasienten en ny stigning i pancreasenzymer fra 6. døgn parallelt med at hun ble ekstubert og sederingen opphevet. CT av pancreasregionen med kontrast er indisert for å vurdere graden av pancreasødem og nekrose (4). MRCP og/eller ERCP benyttes for å påvise gallestein som mulig årsak til akutt pankreatitt. Til tross for gjentatt CT abdomen, MR pancreas og MRCP ble ikke radiologiske forandringer i pancreas påvist hos vår pasient.
Kvinnen var preget av betydelige lungekomplikasjoner med utvikling av bilaterale diffuse fortetninger, dyspné, takypné og hypoksemi som krevde respiratorbehandling. Dessuten forelå tegn på organsvikt uttrykt ved hypotensjon. Lungeaffeksjon er beskrevet som en hyppig komplikasjon til akutt alvorlig pankreatitt og varierer fra mild hypoksemi, atelektase eller pleuraeffusjon via akutt lungeskade til sjokklunge (6). Sjokklunge er sjelden i forløpet av mild pankreatitt. Ved alvorlig pankreatitt er forekomsten av akutt lungeskade/sjokklunge imidlertid 25 – 50 %, og sjokklunge forårsaker over halvparten av dødsfallene i tidlig fase av pankreatitt (7).
Ved akutt alvorlig pankreatitt utvikles flerorgansvikt som likner på bildet ved alvorlig sepsis og store brannskader. Lokal inflammasjon og nekrose fører til frigjøring av toksiske metabolitter. Dette fører videre til utvikling av et systemisk inflammatorisk respons-syndrom (SIRS) som skyldes aktivering av cytokiner, endotoksiner, nøytrofile granulocytter, kjemokiner, adhesjonsmolekyler og andre inflammasjonsmolekyler (2, 8). Hvis ascites fra rotter med eksperimentelt utløst pankreatitt blir injisert intravenøst i friske forsøksdyr, kan lungeskade og utvikling av sjokklunge påvises i alle dyrene innen 24 timer etter injeksjonen (9). Viktige trinn i arakidonsyremetabolismen og inflammasjonsprosessen som aktivering av fosfolipase A₂ (1), syklooksygenase-2 (COX-2) (10) og økt produksjon av proinflammatoriske cytokiner som tumornekrosefaktor-α og interleukin-1 (11) er involvert i lungemanifestasjonene ved akutt pankreatitt.
Behandlingen av akutt pankreatitt er i hovedsak konservativ. Korrigering av væske og elektrolytter, adekvat analgesi, tilfredsstillende ernæring samt standard intensivbehandling av kardiovaskulære, pulmonale, renale og septiske komplikasjoner er viktige tiltak (1, 12). Total parenteral ernæring er nå i økende grad erstattet med enteral ernæring via en jejunumsonde som enten legges ned under røntgengjennomlysning eller endoskopisk (13). Randomiserte studier har vist at dette er godt tolerert, uten kliniske ulemper og assosiert med færre komplikasjoner, spesielt infeksjoner (4, 13). Enteral ernæring er dessuten kostnadsbesparende (13). Forsøk er også gjort med ernæring via ventrikkelsonde (14), men sikkerheten ved slik behandling er ennå ikke klarlagt. Det foreligger ikke sikker dokumentasjon for spesifikk terapi utover endoskopisk behandling ved gallesteinspankreatitt samt perkutan drenasje eller kirurgisk behandling ved infisert nekrotiserende pankreatitt (1, 4, 12).
Antibiotika skal ikke gis rutinemessig ved akutt pankreatitt, men ved CT-påvist pancreasnekrose (steril nekrose) anbefales bredspektret antibiotikadekning profylaktisk (1). Ved påvist infeksjon/infisert nekrose anbefales målrettet antibiotikabehandling. Behandling av lungekomplikasjoner vil ofte inkludere bruk av respirator.
Vår pasient hadde lungekomplikasjoner kombinert med et klinisk og biokjemisk bilde på akutt pankreatitt, med forhøyede serumnivåer av pancreasamylase og lipase. Vi kan ikke se at denne type lungeskade er beskrevet uten samtidig påvisning av ødem eller nekrose av pancreas dokumentert ved CT. Likevel anser vi pasientens pankreatitt som den mest sannsynlige forklaring på hennes lungeaffeksjon. Alvorlige lungekomplikasjoner kan således også oppstå ved mildere former for akutt pankreatitt uten nekrose eller radiologisk påvisbart ødem. Systemiske komplikasjoner ved akutt pankreatitt må identifiseres tidlig slik at adekvat behandling kan iverksettes og risikoen for fatal utgang reduseres.
Etablerte diagnostiske kriterier for akutt pankreatitt er magesmerter samt amylasestigning til mer enn tre ganger øvre referansegrense (eventuelt over 1 000 IE/l). Alternativt kan man stille diagnosen ved magesmerter og tegn til pankreatitt på CT av abdomen. En forhøyet amylase kan normaliseres relativt raskt, og noen sykehus bruker lipase som mål på pankreatitt, da denne holder seg forhøyet i noe lengre tid. Man kan også måle amylase i urin.
Akutte pankreatitter deles inn i lette (75 – 85 %) og alvorlige (15 – 25 %). Klassifiseringen baseres på forskjellige systemer, hvorav Ransons kriterier er de eldste og de som oftest refereres i artikler. Systemet er basert på indikatorer som puls, blodtrykk, leukocytter, trombocytter samt en klinisk vurdering. Alternative skåringssystemer er Imries kriterier, Apache II-kriteriene, samt grad av CRP-stigning. Disse systemene er utviklet for å diagnostisere organsvikt, mens Baltazars skåre er basert på at en ved CT med kontrast evaluerer morfologiske forandringer i pancreas. Det enkleste skåringskriteriet er måling av CRP, som indikerer alvorlig pankreatitt når konsentrasjonen er over 120 mg/l 24 timer etter debut eller over 200 mg/l 48 timer etter debut. Flere studier viser at disse kriteriene skiller godt mellom alvorlig og lett pankreatitt og samstemmer godt med Ransons kriterier.
Pasienten fra Ullevål universitetssykehus hadde en nærmest normal CRP flere dager etter symptomdebut. Sensitivitet og spesifisitet av klassifikasjonssystemene varierer, og når de ikke er 100 %, indikerer det at noen pasienter vil klassifiseres feil. Det gjaldt tydeligvis pasienten fra Ullevål, ettersom hun åpenbart hadde en alvorlig sykdom vurdert ut fra komplikasjonene. Man må likevel anta at det er svært sjelden det oppstår organsvikt når det ikke finnes forandringer i pancreas som kan påvises ved CT med kontrast.
Lankisch og medarbeidere (1) har publisert en interessant prospektiv sammenlikning av ulike diagnostiske skåringssystemer. CT med kontrast og vurdering etter Baltazar-systemet samsvarte best med utvikling av systemiske komplikasjoner i henhold til Atlanta-kriteriene. Av 46 pasienter med Baltazar-skåre 0 (ingen forandringer ved CT), hadde ingen behov for respirator og ingen utviklet organsvikt.
Andersen og medarbeidere anfører at antibiotikaprofylakse kun skal gis til pasienter med tegn på infeksjon. Man taler da ikke om profylakse, men om behandling. Det finnes flere studier vedrørende antibiotikaprofylakse ved alvorlig pankreatitt. Felles for alle randomiserte studier er at de er små og har dårlig teststyrke. Resultater fra en metaanalyse av randomiserte studier viser at man ved profylaktisk antibiotika reduserer forekomst av alvorlige infeksjoner, kirurgiske intervensjoner samt liggedøgn ved intensivavdeling (2). Man fant også en redusert mortalitet som ikke kom frem i enkeltstudiene. Vi kan derfor ikke støtte konklusjonen til Andersen og medarbeidere om at det ikke skal gis profylakse.
Ulike antibiotika har ulik penetrasjon til pancreas eller peripankreatisk væske. Kefalosporiner og makrolider har god penetrasjon, mens den ikke er tilfredsstillende for aminoglykosider. Dersom man bruker profylakse, bør man derfor bruke et antibiotikum med dokumentert god penetrasjon. Vi har god erfaring med bruk av imipenem, selv om det ved alle bredspektrede antibiotika foreligger risiko for soppinfeksjon.