Trombocytopeni er definert som trombocyttmengde < 150 · 109/L og forekommer hyppig hos kritisk syke pasienter. Tilstanden utvikles som følge av redusert produksjon, økt destruksjon eller økt forbruk av trombocytter. Hos kritisk syke pasienter er det ofte flere patofysiologiske mekanismer som forårsaker trombocytopeni, og det er nødvendig å påvise disse for å kunne forutsi forløpet og gi riktig behandling.
Trombocytopeni forekommer hyppig hos kritisk syke pasienter, og ofte er det flere bakenforliggende årsaker. Artikkelen gir en oversikt over trombocytopeni hos kritisk syke, inkludert patofysiologiske mekanismer, forløp, utredning og forslag til behandling. Artikkelen er basert på ikke-systematiske litteratursøk i PubMed-databasen og egen klinisk erfaring.
Forekomst og definisjon
Insidens og prevalens av trombocytopeni varierer avhengig av studiepopulasjon, sykehusavdeling og hvilke definisjoner man legger til grunn (1). I en fersk klinisk studie av trombocytopeni hos pasienter i intensiv- og overvåkningsavdelinger ble trombocytopeni definert som mild (100–149 · 109/L), moderat (51–99 · 109/L) eller alvorlig (< 50 · 109/L), og man fant en insidens på henholdsvis 15,3 %, 5,1 %, og 1,6 % (2). Insidensen av nyoppstått trombocytopeni hos pasienter som er inneliggende i intensivavdelinger, varierer fra 14 % til 44 % (1, 3). Over halvparten av dem som ligger lenger enn to uker i en intensivavdeling, utvikler trombocytopeni, som er assosiert med høy dødelighet (4).
Patofysiologiske mekanismer
Trombocytter produseres i beinmargen fra megakaryocytter, har en levetid på 8–10 dager og brytes i hovedsak ned i milten (5). De er avgjørende for hemostase og bidrar også i angiogenese og medfødt immunitet (5). Årsaker til trombocytopeni kan deles i tre hovedgrupper: redusert produksjon, økt destruksjon og økt forbruk av trombocytter. Ofte kan samme pasient ha flere av disse patofysiologiske mekanismene samtidig (figur 1). Dysfunksjonelle trombocytter er relativt vanlig hos kritisk syke pasienter og kan skyldes uremi, leversvikt, medikamenter og bruk av hjerte- og lungemaskin (6).
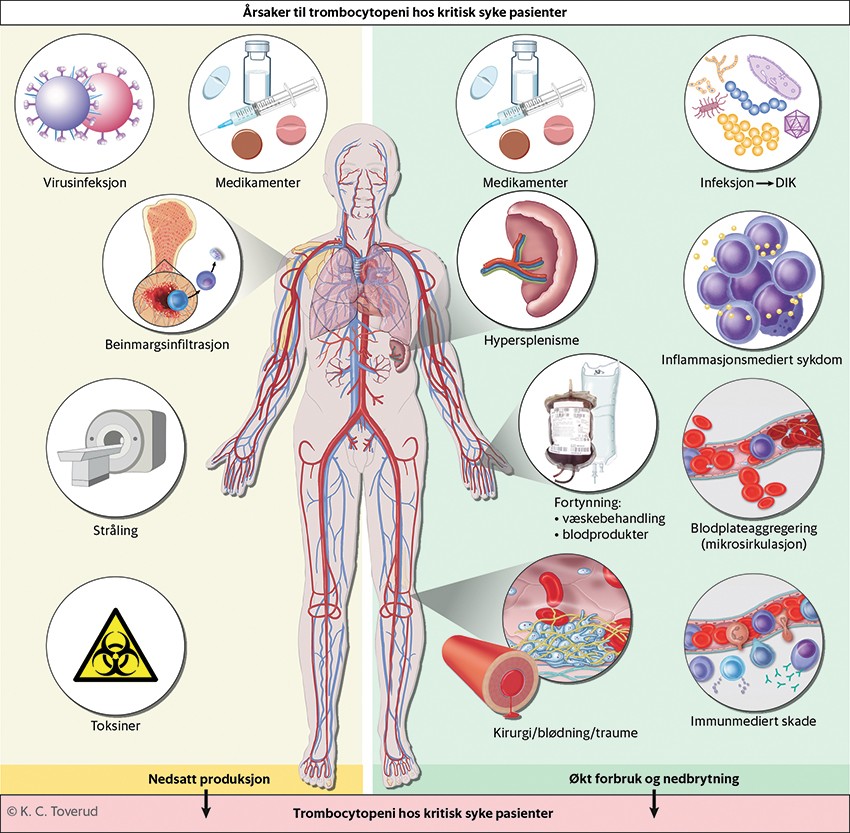
Figur 1 Trombocytopeni er vanlig hos kritisk syke pasienter, og ofte bidrar flere ulike patofysiologiske mekanismer. Årsakene kan deles i tre hovedgrupper: redusert produksjon (beinmargssykdom, bruk av kjemoterapi eller stråleterapi, akutte og kroniske virusinfeksjoner og forgiftninger); økt forbruk av blodplater (fysiologisk aktivering av blodplater ved kirurgi/traume/blødning, patologisk aktivering av blodplater som ved disseminert intravaskulær koagulasjon (DIK), som oftest er utløst av alvorlig infeksjon/sepsis) og økt nedbrytning av blodplater (hypersplenisme, immunologiske medikamentreaksjoner og dannelse av autoantistoffer, inflammasjonsmediert sykdom, som for eksempel hemofagocytisk lymfohistiocytose, og blodplateaggregering i mikrosirkulasjon som ved trombocytisk mikroangiopati). I tillegg kan det oppstå trombocytopeni som følge av en fortynningseffekt ved massiv transfusjon av væske eller blodprodukter.
Nedsatt produksjon
Det er uklart i hvilken grad nedsatt produksjon av trombocytter bidrar til trombocytopeni hos kritisk syke pasienter. Beinmargssykdom eller tidligere behandling med cytotoksisk kjemoterapi reduserer produksjonen av trombocytter. Det samme gjør akutt alkoholtoksisitet. Både akutte og kroniske virale infeksjoner, inkludert hepatitt C-virus, cytomegalovirus, Epstein-Barr-virus og parvovirus B19, kan hemme produksjonen av trombocytter (7). Trombocytopeni er også beskrevet hos pasienter med alvorlig covid-19 (8).
Økt forbruk
Trombocytter kan aktiveres av leukocytter, komplementsystemet, koagulasjonsfaktorer, mikrober eller vevskade. De spiller også en viktig rolle i immunresponsen (9). Trombinmediert aktivering av trombocytter kan være fysiologisk, som ved større kirurgiske inngrep, traume og blodtap. Patologisk aktivering av trombocytter forekommer ved disseminert intravaskulær koagulasjon (DIK) (10), som kan utløses av for eksempel sepsis eller malignitet (11). Aktiverte trombocytter fjernes raskt fra sirkulasjonen, med trombocytopeni til følge. Pasienter som mottar behandling med ekstrakorporal sirkulasjon, har også et økt forbruk av trombocytter og utvikler ofte trombocytopeni.
Økt nedbrytning
Over halvparten av tilfellene med trombocytopeni hos kritisk syke skyldes sepsis eller alvorlig infeksjon (12). Immunologiske medikamentreaksjoner som kan forårsake trombocytopeni, er beskrevet både ved bruk av antitrombotiske medikamenter og antibiotika (13). Samlet forekommer dette hos omkring 15 % av pasientene med trombocytopeni i intensivavdelinger (12). Dannelse av antistoffer kan også føre til trombocytopeni. Vanligst er antistoffer mot heparin–platefaktor 4 (PF4)-komplekset, som medfører heparinindusert trombocytopeni (HIT) ved antikoagulasjonsbehandling med hepariner. Dette er likevel forholdvis sjelden og rapportert hos < 5 % av pasienter med trombocytopeni i intensivavdelinger (14).
Autoantistoffer ved immunologisk trombocytopeni (ITP) er en uvanlig årsak til nyoppstått trombocytopeni hos kritisk syke, men kan også være kjent fra tidligere (15). Alloantistoffer, som kan gi posttransfusjonspurpura, er ekstremt sjelden. Trombotisk trombocytopenisk purpura (TTP) kan være kongenital eller sekundært ervervet (16). Hemofagocytisk lymfohistiocytose (HLH) er en svært alvorlig hyperinflammatorisk tilstand med lymfocytt- og makrofagaktivering, der trombocytopeni kan være en del av sykdomsbildet (17, 18).
Utredning, diagnostikk og forløp
Sammen med målrettet laboratoriediagnostikk er grundig sykehistorie og kartlegging av det kliniske forløpet ofte tilstrekkelig for å finne underliggende årsak til trombocytopeni. Omkring 25 % av kritisk syke pasienter med trombocytopeni har mer enn én bakenforliggende årsak (12) (figur 1). Det er avgjørende å få oversikt over pasientens tidligere sykdommer, komorbiditet og medikamenter og sette dette sammen med den aktuelle kliniske tilstanden. Man må forsøke å avgjøre om trombocytopeni skyldes aktuell kritisk sykdom med organsvikt, eller er en del av en forutgående grunntilstand, som for eksempel alvorlig malign hematologisk sykdom.
Videre bør man vurdere det absolutte platetallet samt utviklingen og forløpet av trombocytopeni. Spesifikke mønster vil da ofte kunne gjenkjennes og indikere underliggende årsak (tabell 1). Generelt vil en kronisk underliggende årsak sammen med nytilkomne årsaker gi en mer alvorlig trombocytopeni (< 50 · 109/L), og stigning i trombocyttall etter trombocyttransfusjon kan utebli. På grunn av høy omsetning gir lave trombocyttall ved kritisk sykdom sannsynligvis en lavere hemostatisk risiko enn trombocytopeni grunnet beinmargssvikt (19).
Tabell 1
Tabellen beskriver typiske forløp av trombocytopeni hos kritisk syke pasienter og mulige årsaker (4).
|
Forløp
|
Sannsynlig årsak
|
|
Platetallet er lavt og forblir lavt
|
Beinmargssvikt
Hypersplenisme
|
|
Raskt fall i platetall som normaliseres raskt
|
Kirurgi
Bruk av hjerte-lunge-maskin
Massive transfusjoner uten trombocytter
|
|
Gradvis fall og normalisering i platetall når den kliniske tilstanden bedres
|
Sepsis
Pankreatitt
Inflammatoriske tilstander
|
|
Platetallet faller og forblir lavt tross klinisk bedring hos pasienten
|
Medikamentutløst trombocytopeni
|
|
Platetallet faller og forblir lavt hos pasienter med persisterende organsvikt
|
Sepsis
Disseminert intravaskulær koagulasjon (DIK)
Sirkulasjonssvikt
|
Man bør også være oppmerksom på andre faktorer som kan bidra til at man måler et lavt trombocyttall. Eksempler er pseudotrombocytopeni på grunn av aggregater av plater i EDTA-blod, hemodilusjon ved væskeinfusjon, massive transfusjoner av andre blodkomponenter uten trombocytter eller opphopning av trombocytter i milten ved splenomegali eller leversykdom med portal hypertensjon. Ved tromboembolisk sykdom hos en pasient med trombocytopeni bør man undersøke for prokoagulatorisk tilstand.
Behandling
Trombocytopeni eller et raskt fall i trombocytter hos kritisk syke pasienter er en markør for dårlig prognose og økt mortalitet. Pasientens underliggende tilstand må behandles. Dersom trombocytopeni er forårsaket av sepsis, må man prioritere infeksjonskontroll og organstøttende behandling (20), men dersom trombocytopeni skyldes massiv blødning, er hemostase og blodtransfusjoner adekvat behandling.
Det er avgjørende å kjenne til de underliggende årsakene for å kunne gi riktig behandling. Transfusjon av trombocytter kan være riktig ved tilstander som reduserer produksjonen eller øker forbruket og nedbrytningen av trombocytter, mens det samtidig er potensielt skadelig ved tilstander med økt intravaskulær aktivering av trombocytter, som heparinindusert trombocytopeni, trombotisk trombocytopenisk purpura og protrombotisk disseminert intravaskulær koagulasjon (21, 22). Transfusjon av trombocytter kan øke forekomsten av sykehusinfeksjoner og transfusjonsassosierte lungeskader (23–25). Dette gir grunn til å ha en konservativ holdning til trombocyttransfusjon og heller legge mer vekt på behandling av grunntilstanden.
Terapeutisk transfusjon
For å unngå alvorlig trombocytopeni og hemodilusjon av koagulasjonsfaktorer behandles alvorlige blødninger med balansert transfusjon med 1: 1: 1-ratio eller 1: 2: 1-ratio med røde blodceller, plasma og trombocytter. Den optimale ratioen av trombocytter i denne behandlingen er usikker (26), og flere steder bruker man transfusjon av fullblod ved alvorlige blødninger (27). Etter internasjonale retningslinjer bør man vurdere transfusjon av trombocytter til kritisk syke pasienter med blødning og samtidig trombocyttall < 50 · 109/L eller det er mistanke om/bekreftet nedsatt trombocyttfunksjon (20, 25).
Profylaktisk transfusjon
Trombocyttransfusjon til kritisk syke pasienter blir oftest gitt for å forebygge og unngå blødninger. Det er betydelig variasjon i klinisk praksis, men internasjonale retningslinjer anbefaler trombocyttransfusjon ved platetall < 10 · 109/L (20, 25). Det er anslått at transfusjon av trombocytter vil øke platetallet med om lag 15 · 109/L per transfusjonsenhet (19), men her er det relativt stor variasjon.
Prosedyrerelatert transfusjon
Transfusjon av trombocytter er anbefalt for å minimere risikoen for blødning ved enkelte prosedyrer, for eksempel ved anleggelse av sentralt venøst kateter og trombocytttall < 20 · 109/L (25, 28). Det finnes likeså retningslinjer og anbefalinger for absolutte platetall ved spinalpunksjon og epiduralanestesi (> 50 · 109/L), større kirurgi (> 50 · 109/L) og nevrokirurgi (> 100 · 109/L). Anbefalingene beror i stor grad på klinisk erfaring, og evidensen er lav (25).
Andre behandlingsmodaliteter
Medikamenter kan påvirke produksjonen og nedbrytningen av trombocytter. Hos kritisk syke kan steroider gis om man mistenker immunologisk genese for lave trombocytter.
Konklusjon
Trombocytopeni er en hyppig tilstand hos kritisk syke pasienter. Ofte skyldes den et samspill av flere ulike patofysiologiske mekanismer som sammen reduserer produksjonen, øker destruksjon og øker forbruket av trombocytter. Den viktigste årsaken er sepsis eller infeksjon. Trombocytopeni er en markør for dårlig prognose og økt dødelighet hos intensivpasienter. Grundig sykehistorie og kartlegging av det kliniske forløpet sammen med målrettet laboratoriediagnostikk er ofte tilstrekkelig for å finne underliggende årsak. Dette er nødvendig for å kunne estimere forløpet og gi riktig behandling. Behandling av underliggende årsak er viktigst, mens trombocyttransfusjoner i hovedsak brukes for å unngå blødningskomplikasjoner inntil man har fått økt trombocyttallet og normalisert hemostasen.
